El diagnóstico genético preimplantacional (DGP) es un análisis genético de los embriones obtenidos de una fecundación in vitro (FIV). Su objetivo es seleccionar aquellos embriones sanos y con capacidad de implantación.
Además, el DGP es la técnica más indicada para evitar la transmisión de una enfermedad genética hereditaria. Gracias al DGP es posible detectar los embriones con mutaciones en su ADN, los cuales serán descartados para su transferencia al útero.
El DGP debe ser realizado por expertos tanto en embriología como en genética, pues requiere hacer técnicas muy delicadas como la biopsia de blastómera y técnicas de genética molecular.
A continuación tienes un índice con los 10 puntos que vamos a tratar en este artículo.
- 1.
- 2.
- 2.1.
- 2.2.
- 3.
- 3.1.
- 3.2.
- 4.
- 4.1.
- 4.2.
- 5.
- 6.
- 6.1.
- 6.2.
- 6.3.
- 6.4.
- 6.5.
- 6.6.
- 6.7.
- 6.8.
- 6.9.
- 6.10.
- 7.
- 8.
- 9.
- 10.
DGP paso a paso
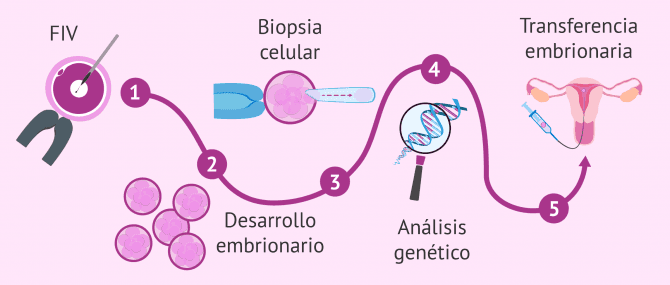
La FIV con DGP es uno de los tratamientos más laboriosos de reproducción asistida. Por ello, este tratamiento de fertilidad cuenta con varios pasos desde la estimulación ovárica hasta la transferencia embrionaria. A continuación, se comentan cada uno de ellos:
- FIV
- consiste en hacer una estimulación ovárica a la mujer, obtener los óvulos mediante punción folicular y, finalmente, fecundar los óvulos con los espermatozoides de la pareja masculina o de un donante anónimo.
- Desarrollo embrionario
- día a día se valoran las características de los embriones en cultivo, ya que para hacer la biopsia es necesario que cuenten con unos mínimos de calidad que aseguren su supervivencia.
- Biopsia celular
- extracción de una o varias blastómeras (células del embrión) para su posterior análisis genético. Se puede realizar en embriones de día 3 o una vez hayan conseguido el estado de blastocisto en día 5. A continuación, la célula extraída se coloca en un tubo con sumo cuidado, proceso conocido como tubing.
- Análisis genético
- estudio de los cromosomas y/o genes de las células biopsiadas para identificar posibles alteraciones en ellos. Concretamente, el análisis de cromosomas es más conocido como cribado genético preimplantacional y, por otra parte, el término DGP se utiliza para el análisis de mutaciones genéticas concretas.
- Transferencia embrionaria
- se seleccionan los embriones genéticamente sanos para transferirlas al útero materno o criopreservarlos para futuros intentos.
La transferencia de embriones puede hacerse en fresco o en ciclo diferido. Esto dependerá del tiempo necesario para la obtención de los resultados del análisis genético, siendo bastante habitual que los embriones tengan que congelarse.
Biopsia embrionaria
La biopsia embrionaria es el proceso de extracción de una o varias células, llamadas blastómeras. Así se puede analizar el ADN de los embriones en busca de alguna alteración genética.
La viabilidad del embrión puede verse comprometida con esta biopsia, ya que el hecho de perder una célula puede suponer demasiado estrés para él y que no sobreviva. Por ello, es necesario que esta extracción celular sea realizada por personal de laboratorio altamente especializado y con experiencia.
Es posible calcular TU probabilidad de implantación según el tratamiento, edad y otros factores?
Porque sí, tener endometriosis, SOP, baja reserva ovárica, falta u obstrucción de las tompas, así como la calidad del semen condicionan tus probabilidades de embarazo.
Puedes personalizar tu informe de fertilidad en 2 minutos.
La biopsia embrionaria puede hacerse en día 3 o en día 5. En ambos casos, es imprescindible que la fecundación tenga lugar a través de una ICSI.
En la FIV convencional, hay espermatozoides y células de la granulosa adheridos a la zona pelúcida del embrión. Esto supone un riesgo de contaminación de las blastómeras extraídas y, por tanto, el DGP podría dar un resultado alterado.
Biopsia de blastómera en día 3
Al tercer día de desarrollo embrionario, los embriones de buena calidad suelen tener 8 células, aunque también pueden tener un número entre 6 y 10 células en función de su ritmo de división.
Por esta razón, si la biopsia se hace en este preciso momento, solamente se extraerá una sola blastómera del embrión, o como máximo 2, con el fin de no comprometer su viabilidad.
Durante el procedimiento, se realiza un orificio en la zona pelúcida del embrión mediante pulsos de láser o agentes químicos, como el ácido Tyrodes. Una vez realizado este orificio, se extrae la blastómera por aspiración.
Después de la biopsia embrionaria, existen dos opciones posibles para los embriones:
- Cultivo a blastocisto
- los embriones se dejan en cultivo para que continúen su evolución mientras se esperan los resultados del análisis genético. Por tanto, la transferencia embrionaria será en estado de blastocisto en día 5.
- Vitrificación de embriones
- los embriones se congelan después de la biopsia para ser transferidos en un ciclo posterior.
Si te interesa leer más sobre este tema, puedes acceder al siguiente post: Transferencia de embriones congelados.
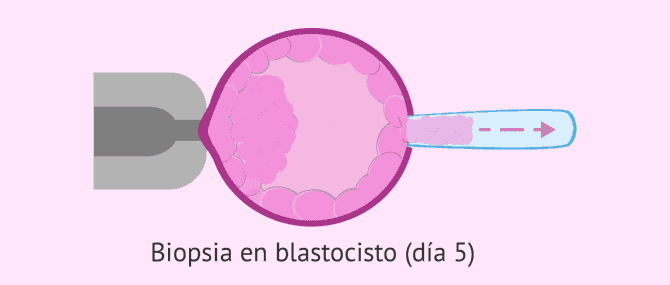
Biopsia de trofoectodermo en día 5
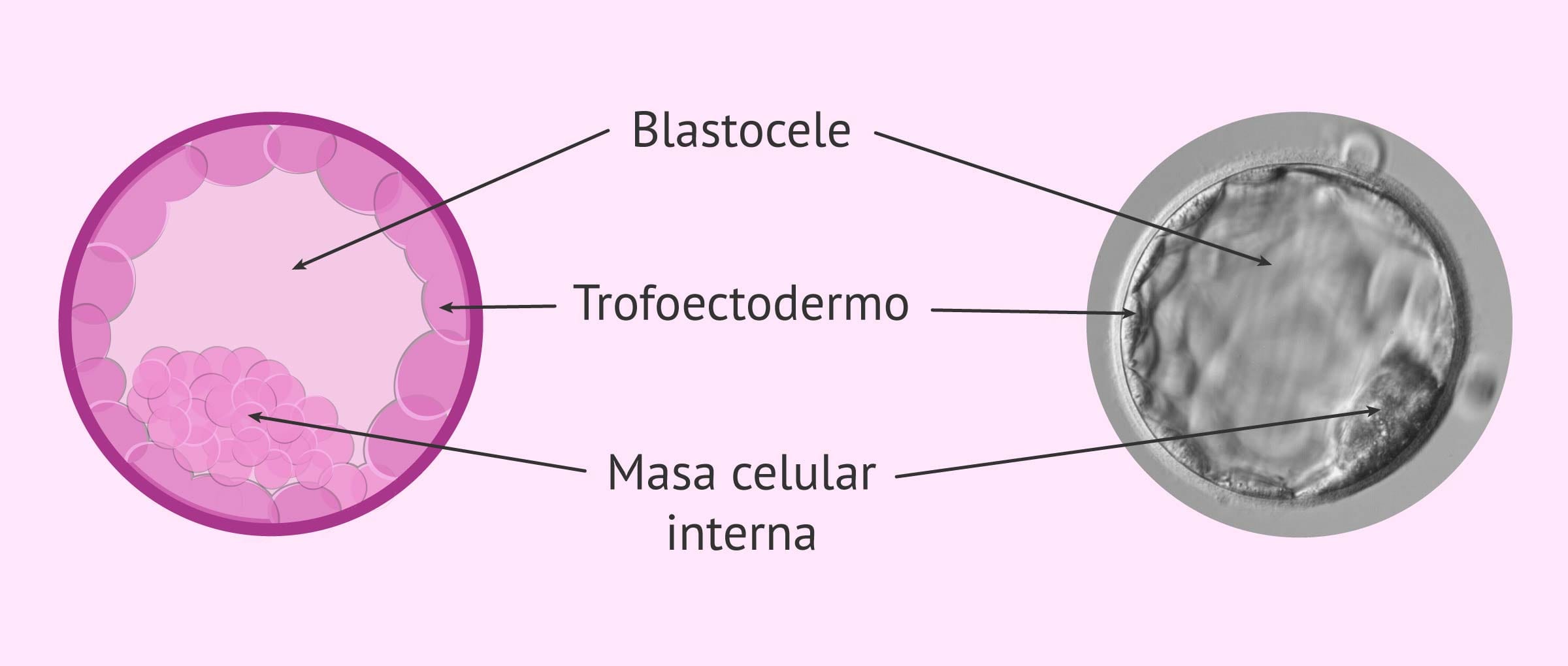
Al quinto día de desarrollo, el embrión ya se ha convertido en lo que se conoce como blastocisto. Éste es un embrión más grande, compuesto por multitud de células y con 3 partes diferenciadas:
- Masa celular interna (MCI)
- da lugar al futuro feto.
- Blastocele
- es una cavidad interna llena de líquido.
- Trofoectodermo
- capa externa que origina la placenta y otras estructuras extraembrionarias.
Aunque se trata de poblaciones celulares diferentes, tanto las células de la MCI como del trofoectodermo tienen el mismo material genético. Por tanto, es posible extraer unas pocas células de esta capa externa para analizarlas con el DGP.
El hecho de poder extraer varias células del embrión supone una ventaja, ya que se obtendrá un resultado más fiable, será posible detectar los casos de mosaicismo y, además, la viabilidad del embrión no se verá tan comprometida.
A la hora de hacer la biopsia con un blastocisto, es necesario tener la precaución de hacer el orificio en un lugar alejado de la MCI con el objetivo de evitar posibles daños.
Por otra parte, es más conveniente utilizar los pulsos cortos del láser para agujerear la zona pelúcida que el ácido Tyrodes, ya que ésta ha reducido mucho su espesor al expandirse el blastocisto y el uso de un agente químico podría dañarlo.
A continuación, una vez hecho un orificio suficiente para introducir la pipeta de la biopsia, se extraen las células por aspiración. Para separar las células que se quieren extraer de las que se quedan en el interior del embrión, los pulsos de láser pueden ayudar.
En este caso, sí será necesario vitrificar los embriones después de la biopsia para transferirse en un futuro ciclo, ya que los resultados del análisis genético tardan varios días y no sería viable dejar los embriones en cultivo.
Puedes obtener más información sobre esto en el siguiente artículo: Las tasas de implantación de los blastocistos congelados.
Cribado genético preimplantacional
El cribado genético preimplantacional, también conocido como PGS por su nombre en inglés (Preimplantation Genetic Screening), es un tipo de DGP en el que se analizan las posibles aneuploidias en los embriones.
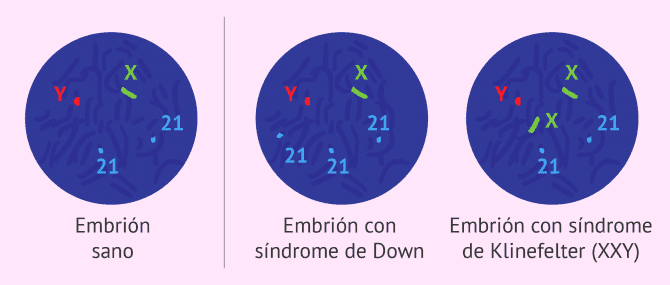
Las aneuploidias son las alteraciones en el número o en la estructura de los cromosomas, teniendo en cuenta que la dotación cromosómica normal del ser humano es de 46 cromosomas.
La ganancia o la pérdida de un cromosoma, así como cambios en su estructura, son anomalías que pueden dar lugar a embriones no viables o a recién nacidos con cromosomopatías como el síndrome de Down.
En algunas clínicas, este tipo de DGP también es llamado screening de aneuploidias y las pruebas genéticas utilizadas para su detección son las que se comentan en los siguientes apartados.
Estudio FISH
La hibridación in situ fluorescente (FISH) es la técnica que se ha utilizado de forma tradicional en el estudio de anomalías cromosómicas.
Únicamente permite analizar ciertas regiones de 9 cromosomas (13, 15, 16, 17, 18, 21, 22, X e Y). No obstante, estos cromosomas están implicados en aneuploidias que pueden dar lugar a abortos de repetición o al nacimiento de niños enfermos.
El proceso consiste en añadir sondas fluorescentes para regiones específicas de los cromosomas que van a analizarse. A continuación, es posible visualizar la señal fluorescente a través de un microscopio especial y detectar si falta alguna de las regiones analizadas o, al contrario, si hay más copias de las que debería.
Puesto que el hecho de analizar solamente un número de cromosomas determinado supone una limitación, la FISH se considera un análisis incompleto y, a día de hoy, está siendo reemplazada por otras técnicas que permiten un análisis genético completo del embrión.
Arrays de CGH
El array de Hibridación Genómica Comparada (A-CGH) es una técnica que permite realizar un Screening Cromosómico Completo (CCS, por su nombre en inglés Comprehensive Chromosome Screening), es decir, se analizan los 23 pares de cromosomas a la vez en busca de regiones con alguna alteración cromosómica.
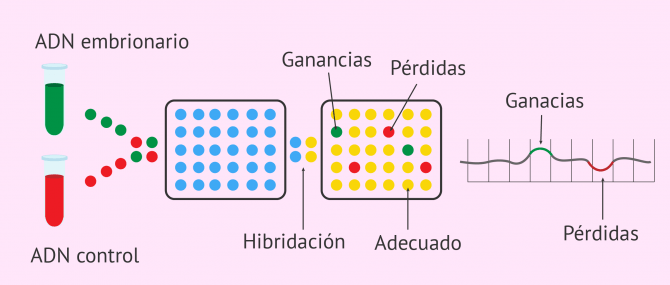
Para llevar a cabo este análisis genético, se emplea un ADN control y la muestra de ADN a estudiar procedente de la célula embrionaria extraída. Ambas hebras de ADN se marcan con sondas fluorescentes diferentes y, a continuación, se hibridan en el microarray.
Con esta metodología se consigue comparar el ADN del embrión con el de la muestra de referencia e identificar pérdidas (deleciones) o ganacias (duplicaciones) de material genético, las cuales podrían conducir a defectos embrionarios.
A pesar de que esta técnica es mucho más resolutiva que la FISH, solo realiza comparaciones cuantitativas, es decir, detecta si falta o sobra material genético. Por tanto, no detecta si hay fragmentos cromosómicos que no estén en el lugar adecuado, como inversiones o traslocaciones.
DGP para enfermedades monogénicas
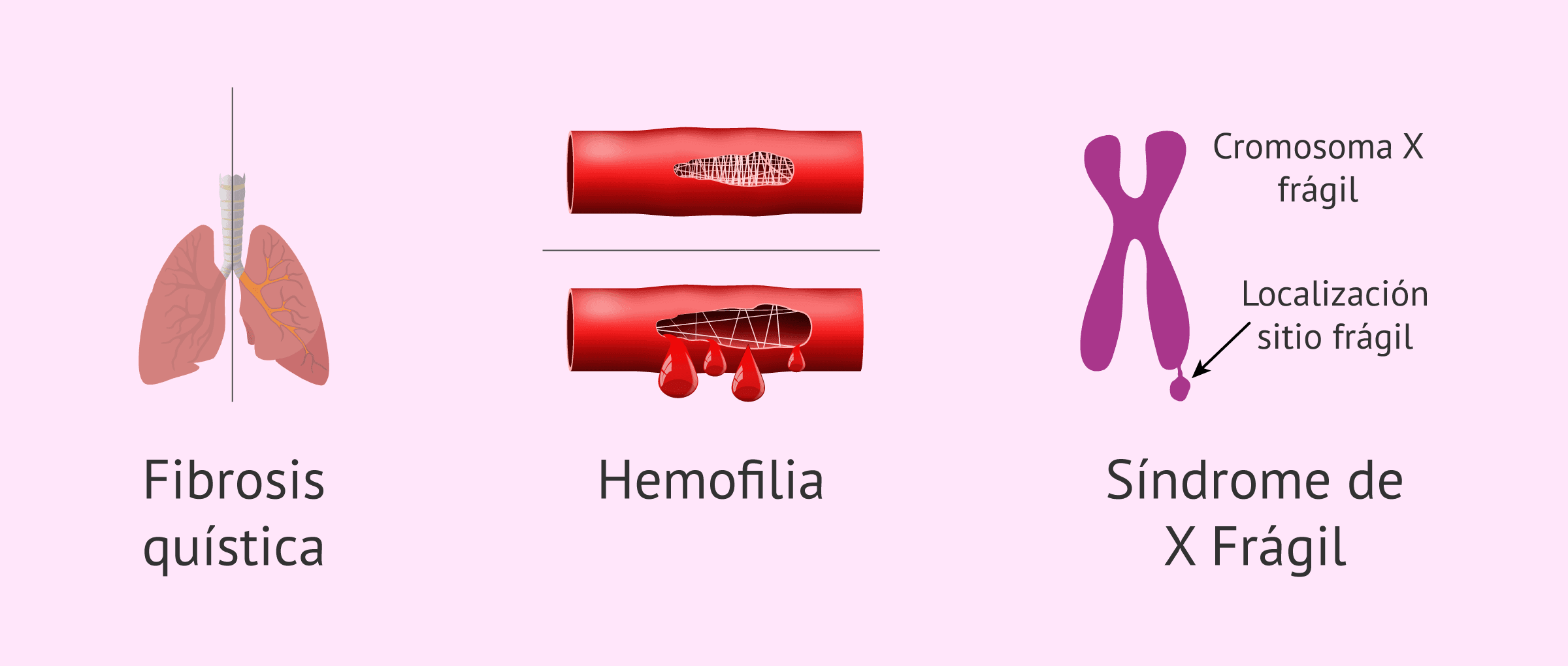
Las enfermedades monogénicas son aquellas causadas por mutaciones en un único gen como, por ejemplo, la fibrosis quística, la hemofilia o el síndrome de X frágil.
Además, son enfermedades hereditarias que se transmiten de padres a hijos. Por ello, antes de hacer el DGP en los embriones, es necesario identificar la mutación concreta en los padres a través de un estudio de informatividad.
Una vez localizada la mutación y determinado el tipo de herencia (dominante, recesiva o ligada al sexo), es posible hacer un estudio a los embriones con las herramientas genéticas que comentamos a continuación.
PCR
La reacción en cadena de la polimerasa (PCR) consiste en la amplificación de secuencias de ADN específicas para su posterior análisis.
Así, es posible obtener millones de copias del gen de interés a partir de una única copia presente en la célula extraída.
Una vez amplificada la secuencia deseada, se utilizan diferentes técnicas de biología molecular para analizarla y localizar las posibles mutaciones que dan lugar a las enfermedades monogénicas.
Secuenciación masiva
La secuenciación masiva o NGS (del nombre en inglés, Next-Generation Sequencing) es la técnica más avanzada a día de hoy para el estudio genético.
Las ventajas que ofrece la secuenciación masiva con respecto a las otras técnicas son las siguientes:
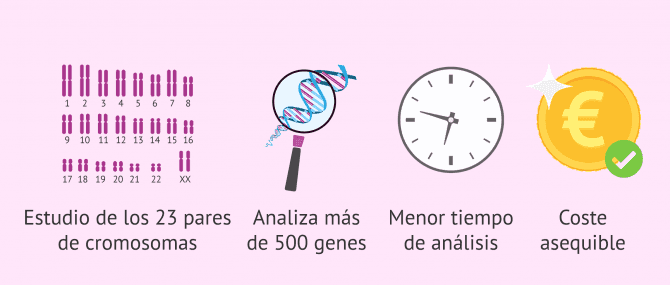
- Permite estudiar los 23 pares de cromosomas en un mismo análisis, y con una mayor resolución.
- Permite analizar simultáneamente más de 500 genes asociados a enfermedades hereditarias.
- Es posible el estudio de aneuploidías y enfermedades monogénicas por separado o de forma simultánea en un único análisis.
- Menor tiempo de análisis, evitando la necesidad de tener que congelar los embriones mientras se esperan los resultados.
- Permite analizar a la vez un alto número de muestras, por lo que el coste del análisis es más asequible.
Actualmente, cada vez son más las clínicas que optan por contar con esta última tecnología tanto para el screening de aneuploidías como para la detección de enfermedades monogénicas.
Transferencia de embriones sanos
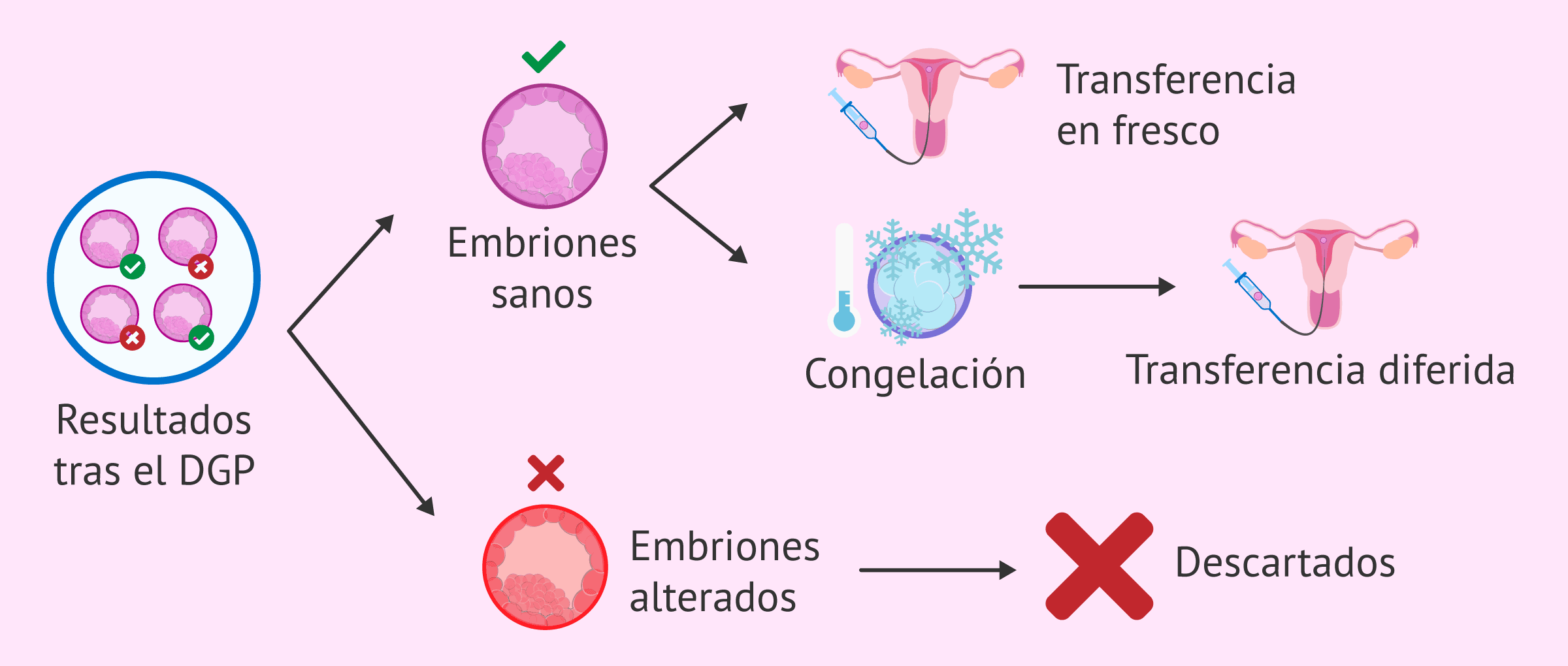
Una vez obtenidos los resultados, los embriones sanos serán transferidos al útero materno o vitrificados para futuros intentos. Los embriones con alteraciones genéticas quedan descartados, aunque aparentemente tengan buena calidad morfológica.
En el caso de haber vitrificado los embriones previamente a los resultados, se transferirán en un ciclo sustituido. Para ello, la mujer tendrá que hacer una preparación endometrial con la administración de estrógenos y progesterona.
Si los resultados muestran que hay varios embriones libres de anomalías, solamente se descongelará aquel embrión o embriones que, además, tengan la mejor calidad morfocinética para ser transferido/s. Esto aumentará la probabilidad de implantación embrionaria y, por tanto, de lograr el embarazo.
Preguntas de los usuarios
¿Qué probabilidad hay de que no queden embriones después del PGT?
El Test Genético Preimplantacional (PGT) permite la detección de anomalías genéticas en los embriones, antes de su transferencia al útero de la mujer. Identificando los embriones libres de anomalías cromosómicas y mutaciones genéticas se puede evitar su transmisión a la descendencia.
Cuantos más embriones haya disponibles para la realización de un PGT, mayores son las posibilidades de obtener embriones sanos aptos para ser transferidos al útero de la mujer. Los avances en el cultivo embrionario y las técnicas de biopsia han permitido que el análisis genético de embriones se realice en la etapa de blastocisto, permitiendo obtener una mayor cantidad de células (trofoectodermo) y manteniendo la integridad del embrión y su capacidad de implantación.
Sin embargo, la reserva ovárica y la respuesta ovárica a la estimulación de gonadotropinas están inversamente relacionadas con la edad materna, ya que a más edad menor reserva y respuesta. En consecuencia, la edad materna avanzada afecta al número de ovocitos, la calidad de los mismos y el número de embriones disponibles para biopsiar.
¿Cuántos embriones se transfieren después de hacer un DGP?
El número de embriones a transferir a una paciente no depende de la técnica que se le haya practicado al embrión, sino del día en el que se encuentra, la calidad del mismo y de las características intrínsecas de cada paciente. La realización de un Diagnóstico Genético Preimplantacional está asociada en la mayoría de los casos a la edad materna avanzada (screening de aneuploidías) o la presencia de patologías genéticas graves (en muchos casos presentes en la mujer). En ambos casos, el embarazo múltiple está contraindicado.
Por todas estas circunstancias, el consejo médico suele ser la transferencia de un solo embrión.
¿En qué tipo de casos se está utilizando el DGP?
El DGP facilita la toma de decisiones informadas y cada vez es más frecuente que se incluya como opción dentro de un correcto asesoramiento genético.
El objetivo actual es que pueda llegar a cualquier pareja, si así lo elige libremente, y a cualquier patología hereditaria, siempre que exista indicación clínica y sea posible abordar su diagnóstico técnicamente.
Respecto a las parejas con antecedentes clínicos por enfermedad monogénica, las indicaciones actuales principales son, entre otras, fibrosis quística, atrofia muscular espinal, distrofia miotónica (Steinert), síndrome X frágil y Huntington.

Respecto al análisis cromosómico, la indicación principal es el estudio embrionario por riesgo de aneuploidías en edad materna avanzada, sin olvidar el grupo de pacientes con antecedentes de aborto recurrente y factor masculino severo.
¿Es lo mismo DGP y PGT?
Son las siglas para denominar los estudios genéticos que se realizan a un embrión antes de ser transferidos al útero. Por un lado el DGP hace referencia al diagnostico genético preimplantancional; mientras que el PGT son las siglas de Test Genético Preimplantacional.
Actualmente, el término más utilizado para denominar a esta técnica complementaria es el PGT.
¿Qué ventajas tiene hacer un PGT?
Cuando no se realiza un PGT (antes conocido como DGP), la selección embrionaria se realiza en base a parámetros morfológicos o morfocinéticos (si el embrión se ha incubado en un sistema time-lapse).
El PGT presenta la ventaja de que permite seleccionar el embrión que se va a transferir al útero según los resultados del análisis genético realizado. Al transferir solo embriones con un resultado favorable, se evita transferir embriones con alteraciones genéticas que podrían dar lugar a un aborto espontáneo o al nacimiento de un bebé con una enfermedad.
¿Extraer una o varias células del embrión puede afectar negativamente a su desarrollo posterior?
Realizar una biopsia al embrión para extraer una o varias células puede considerarse un procedimiento "invasivo" que podría afectar a la supervivencia del embrión. No obstante, la viabilidad del embrión no suele verse comprometida tras la biopsia para el PGT, sobre todo, cuando se realiza en embriones en estadio de blastocisto (día 5 de desarrollo embrionario), ya que los blastocistos tienen más células que los embriones en día 3 de desarrollo.
¿Conoces el test genético preimplantacional no invasivo?
Silvia Azaña, embrióloga en Reproducción Asistida ORG, nos cuenta en este vídeo todos los detalles acerca del test genético preimplantacional no invasivo:
El test genético preimplantacional no invasivo o test Embrace es una técnica que analiza el ADN libre que el embrión va liberando en el medio de cultivo (ese líquido donde permanece mientras se desarrolla en el laboratorio). A partir de ahí, estudiando ese ADN embrionario en el medio de cultivo, se puede obtener información genética del embrión sin necesidad de extraer algunas de sus células (es decir, sin necesidad de biopsiarlo). Por ello, como solo analiza el medio de cultivo en el que se ha desarrollado el embrión (y que habitualmente se desecha), se llama “no invasivo”.
El objetivo del test genético preimplantacional no invasivo es evaluar la probabilidad de que un embrión sea cromosómicamente normal (euploide).Sin embargo, y esto es muy importante que lo sepas, el test Embrace no es un sustituto del PGT, pero sí que es muy útil. Te cuento el por qué.
En función de la probabilidad de ser euploide, es decir, sano, el test Embrace ofrece una clasificación de tus embriones. Así, se prioriza para transferir los embriones con más probabilidades de ser euploides y, por tanto, con más posibilidades de implantar y de dar lugar a un embarazo evolutivo.
Es decir, el test Embrace es una herramienta de gran ayuda en la selección embrionaria, para priorizar los mejores embriones para transferir en tu tratamiento de FIV.
¿Qué decisiones clínicas permite tomar un informe de PGT-A?
El Dr. Manuel Fernández, director médico de Vida Sevilla y director científico de las clínicas Vida, nos cuanta qué decisiones se pueden tomar según el resultado del PGT-A:
La decisión clínica que permite tomar un informe de PGT-A es muy clara. Hay embriones que son anormales cromosómicamente, ¿vale? Técnicamente se llama aneuploides, por eso está la A en el estudio genético preimplantacional-A, de aneuploides, anormales cromosómicamente. Anormales desde el punto de vista del número de cromosomas (trisomía, monosomía, etcétera).
Entonces, esos embriones que son anormales cromosómicamente no se pueden transferir. Y los embriones que son normales cromosómicamente sí se pueden transferir.
Aquí hay un tema muy interesante que seguramente pacientes que están en tratamiento o han hecho tratamiento recientemente estarán un poco más familiarizadas, que es el término mosaicismo. ¿Qué es el mosaicismo? Bueno, digamos que sería el gris. O sea, tenemos embriones que son completamente normales desde punto de vista cromosómico, sería el blanco. Embriones que son completamente anormales del punto de vista cromosómico, son el negro. Los normales se pueden transferir, los que tengan anomalías cromosómicas no se pueden transferir, pero hay un grupo de embriones en los que eso no está tan claro, en el que parece que hay un riesgo ligeramente aumentado, pero probablemente no. Son los embriones que son de mosaicismo. Y dentro de los embriones mosaicos los hay de diferentes grados. Los hay muy probablemente con anomalías y muy probablemente sin anomalías. Entonces, esos embriones que son mosaicos, algunos de ellos se pueden transferir, pero siempre se habla previamente con los pacientes para explicarles por qué estamos en ese gris, porque esos embriones mosaicos no son ni seguro normales cromosómicamente ni seguro anormales cromosómicamente, sino con un riesgo aumentado mucho o poco. Y en función de eso, en cualquier caso, suelen ser los últimos embriones que se transfieren, solamente cuando ya no queda ningún embrión normal para transferir o desde el principio no lo ha habido, y siempre explicando esto a los pacientes para que ellos tengan la última palabra "Oye, pues este embrión con este riesgo aumentado, mucho o poco, preferimos transferírnoslo o no.
¿Es mejor el PGT en día 3 o en día 5?
Actualmente es mucho más frecuente realizar la biopsia embrionaria para el test genético preimplantacional (PGT, antes conocido como DGP) en día 5 de desarrollo embrionario, ya que el embrión en estadio de blastocisto (día 5) tiene un mayor número de células que en día 3 y, por tanto, se pueden extraer una pequeña cantidad de células del trofoectodermo (la parte del embrión que dará lugar a la placenta).
¿Se puede hacer una biopsia de corpúsculo polar?
Sí, sería posible realizar una biopsia del primer corpúsculo polar del óvulo con la finalidad de realizar un análisis genético. Se trataría, en este caso, de un estudio genético preconcepcional (antes de la fecundación del óvulo con el espermatozoide). Por tanto, este estudio del corpúsculo polar podría aportar información del estado genético del óvulo, pero no puede evaluar si el futuro embrión (una vez que se produzca la fecundación) tendrá alguna alteración genética de origen paterno.
Por todo ello, esta técnica no es nada habitual, puesto que lo más común es realizar un test genético preimplantacional (PGT) a los embriones, realizando la biopsia cuando estos están en estadio de blastocisto.
Lectura recomendada
A lo largo de este artículo, hemos comentado que el DGP sirve para detectar anomalías genéticas y cromosómicas en los embriones. Si quieres saber qué enfermedades concretas tienen lugar como consecuencia de estas alteraciones, puedes seguir leyendo aquí: ¿Qué enfermedades genéticas o cromosómicas puede detectar el DGP?
Para obtener información sobre las tasas de éxito de esta técnica, te animamos a entrar en el siguiente artículo: Probabilidad de embarazo con el DGP.
Comunidad y Apoyo
En Reproducción Asistida ORG trabajamos para que la información mensual y rigurosa sea accesible para todos. Si este artículo te ha ayudado, considera apoyarnos para que podamos seguir acompañando a más personas en su camino hacia la maternidad y paternidad.
Bibliografía
Anthony Homer H. Preimplantation genetic testing for aneuploidy (PGT-A): The biology, the technology and the clinical outcomes. Aust N Z J Obstet Gynaecol. 2019 Apr;59(2):317-324. doi: 10.1111/ajo.12960. Epub 2019 Feb 27 (Ver)
Rajesh Parikh F, Sitaram Athalye A, Jagannath Naik N, Jayaram Naik D, Ramesh Sanap R, Fali Madon P. Preimplantation Genetic Testing: Its Evolution, Where Are We Today?J Hum Reprod Sci . Oct-Dec 2018;11(4):306-314. doi: 10.4103/jhrs.JHRS_132_18 (Ver)
Sciorio R, Anderson R. Fertility preservation and preimplantation genetic assessment for women with breast cancer.Cryobiology. 2020 Feb 1;92:1-8. doi: 10.1016/j.cryobiol.2019.12.001. Epub 2019 Dec 18.
Wilding M, Terribile M, Parisi I, Nargund G. Thaw, biopsy and refreeze strategy for PGT-A on previously cryopreserved embryos. Facts Views Vis Obgyn. 2019 Sep;11(3):223-227 (Ver)
Preguntas de los usuarios: '¿Qué probabilidad hay de que no queden embriones después del PGT?', '¿Cuántos embriones se transfieren después de hacer un DGP?', '¿En qué tipo de casos se está utilizando el DGP?', '¿Es lo mismo DGP y PGT?', '¿Qué ventajas tiene hacer un PGT?', '¿Extraer una o varias células del embrión puede afectar negativamente a su desarrollo posterior?', '¿Conoces el test genético preimplantacional no invasivo?', '¿Qué decisiones clínicas permite tomar un informe de PGT-A?', '¿Es mejor el PGT en día 3 o en día 5?' y '¿Se puede hacer una biopsia de corpúsculo polar?'.








Hola, ¿todas las clínicas ofrecen DGP y tienen personal altamente cualificado? Me da miedo que por quitar una celulita al embrión… en el futuro tenga problemas. ¿Pasa algo? Os ruego sinceridad. Gracias.
Hola MamiF,
No todas las clínicas de fertilidad ofrecen la técnica de DGP. Además, algunos centros de reproducción asistida realizan la biopsia embrionaria, pero el análisis lo envían a un servicio externo. La biopsia embrionaria es un proceso delicado y requiere gran habilidad por parte de los especialistas.
Por otro lado, no te debe preocupar el hecho de extraer una célula al embrión para su análisis genético. Al tratarse de un momento muy temprano del desarrollo embrionario, el embrión será capaz de continuar dividiéndose y de compensar la célula extraída.
Si necesitas ayuda para seleccionar una clínica de fertilidad que ofrezca DGP, te recomiendo acceder al Informe de Fertilidad. Se trata de una herramienta gratuita a través de la cual recibirás un listado personalizado de las clínicas de tu zona de interés que cumplen con nuestros criterios de calidad. Además, obtendrás información de precios, servicios incluidos, explicaciones detalladas de los tratamientos y muchas cosas más.
Espero que te sea útil.
Un saludo.