Hoy en día es muy frecuente realizar transferencias embrionarias de embriones vitrificados. Esto se debe, en gran medida, a la evolución de las técnicas de fecundación in vitro (FIV). Entre los principales motivos destacan la necesidad de evitar el síndrome de hiperestimulación ovárica, el aumento en la realización del estudio genético preimplantacional, la incorporación de nuevos protocolos de estimulación —como el uso de progesterona como inhibidor hipofisario— y estrategias como la estimulación en fase lútea (DuoStim). En todos estos escenarios, la vitrificación embrionaria permite posponer la transferencia y realizarla en un ciclo diferido, en condiciones más controladas.
Antes de llevar a cabo cualquier transferencia embrionaria, especialmente en el caso de embriones vitrificados, es imprescindible realizar una adecuada preparación endometrial. El objetivo es sincronizar el endometrio con el estadio de desarrollo embrionario, de modo que la transferencia se produzca en el momento óptimo para favorecer la implantación.
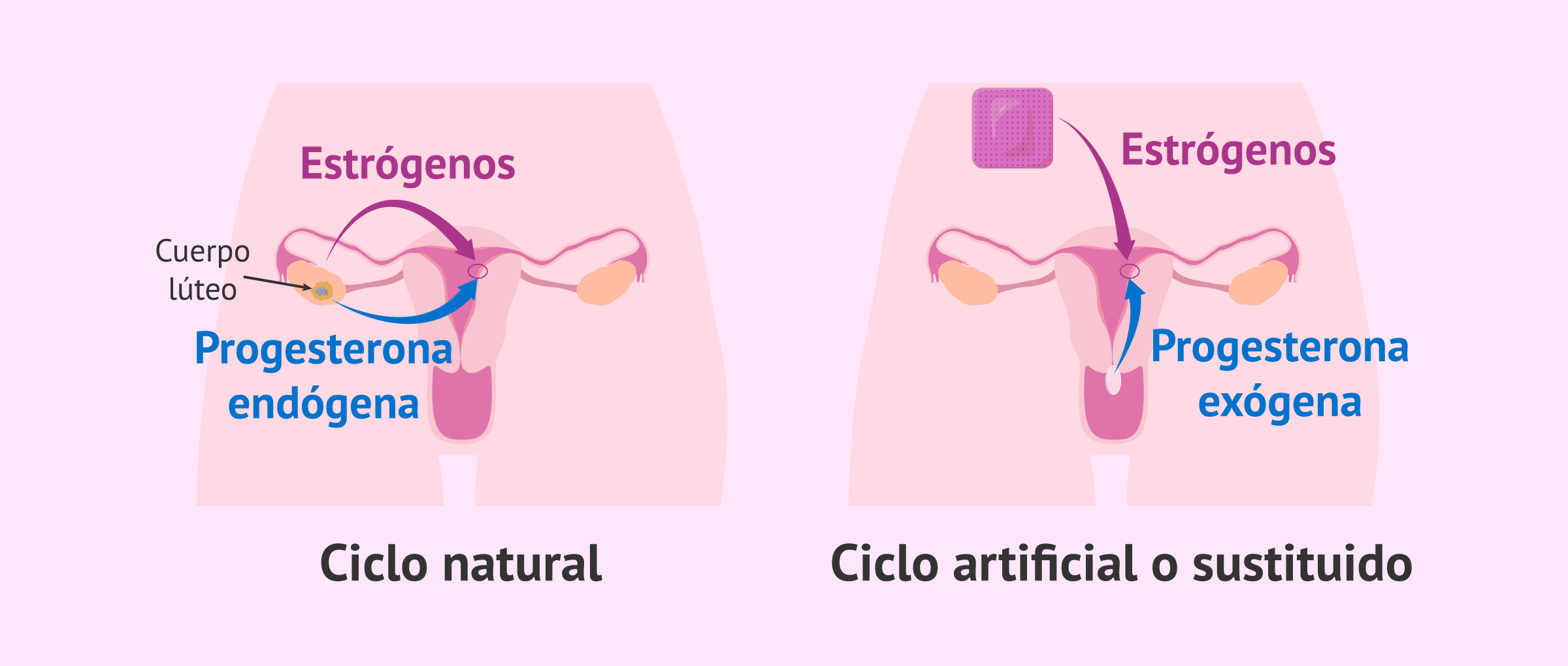
De forma general, existen dos estrategias principales para la preparación endometrial: el ciclo natural y el ciclo artificial o sustituido. En términos de resultados, ambas opciones muestran tasas de gestación similares, por lo que la elección suele basarse en las características de la paciente y en criterios clínicos. La diferencia fundamental radica en la presencia o ausencia de cuerpo lúteo: en el ciclo natural existe cuerpo lúteo, responsable de la producción endógena de progesterona, mientras que en el ciclo artificial este no está presente, lo que obliga a administrar progesterona de forma exógena.
Durante la preparación endometrial se realizan controles ecográficos para valorar el grosor y el patrón del endometrio, así como determinaciones hormonales de estrógenos y progesterona, tanto durante el proceso de preparación endometrial, así como previo a la transferencia embrionaria. En los ciclos artificiales, diversos estudios han demostrado que niveles de progesterona previos a la transferencia superiores a 9,2–10,6 ng/mL se asocian con mejores tasas de gestación, mientras que valores inferiores pueden comprometer los resultados.
Asimismo, estudios recientes indican que la medición de progesterona el día de la determinación de la beta-hCG positiva también tiene valor pronóstico. Niveles superiores a 10,6 ng/mL se relacionan con mejores tasas de recién nacido vivo, y valores por encima de 24 ng/mL parecen asociarse a resultados aún más favorables. En aquellos casos en los que no se alcanzan estos niveles, puede ser recomendable la suplementación con progesterona, siendo la vía subcutánea una de las opciones preferentes.
En los ciclos naturales modificados, donde existe cuerpo lúteo, no parece imprescindible medir la progesterona antes de la transferencia. No obstante, algunos autores recomiendan su determinación tanto en ese momento como el día de la beta-hCG positiva para confirmar una adecuada función lútea y detectar posibles descensos que requieran suplementación adicional.
En cuanto a los estrógenos, su papel es menos determinante durante la implantación y en los primeros días tras esta. En ciclos artificiales, los niveles suelen situarse entre 150 y 500 pg/mL, aunque pueden variar según el protocolo. En el día de la beta-hCG positiva, estos valores pueden oscilar entre 200 y 1000 pg/mL.
En conclusión, la transferencia embrionaria constituye el paso final de un ciclo de FIV y debe individualizarse en cada paciente. La monitorización de la progesterona, tanto antes de la transferencia como tras una beta positiva, permite ajustar el tratamiento y optimizar las probabilidades de éxito.
