El diagnóstico genético preimplantacional (DGP), también conocido como PGT por sus siglas en inglés, es una técnica de prevención que se utiliza en reproducción asistida con la finalidad de detectar anomalías en el material genético de los embriones. Se trata, por tanto, de una técnica complementarias que ayudará a elegir el mejor embrión para transferir en un tratamiento de fecundación in vitro (FIV).
Gracias al DGP, es posible evitar la transferencia de embriones con alteraciones genéticas o cromosómicas y, de esta manera, aumentar la probabilidad de tener un hijo sano.
Esta técnica se puede aplicar en todos los pacientes que se han sometido a un tratamiento de FIV y han conseguido embriones. Pese a ello, hay situaciones en las que se recomienda más hacer DGP para obtener un mejor pronóstico del tratamiento reproductivo.
A continuación tienes un índice con los 12 puntos que vamos a tratar en este artículo.
- 1.
- 2.
- 3.
- 4.
- 5.
- 5.1.
- 5.2.
- 5.3.
- 5.4.
- 6.
- 7.
- 8.
- 8.1.
- 8.2.
- 8.3.
- 8.4.
- 8.5.
- 8.6.
- 8.7.
- 8.8.
- 8.9.
- 8.10.
- 8.11.
- 8.12.
- 8.13.
- 9.
- 10.
- 11.
- 12.
¿Qué es el DGP?
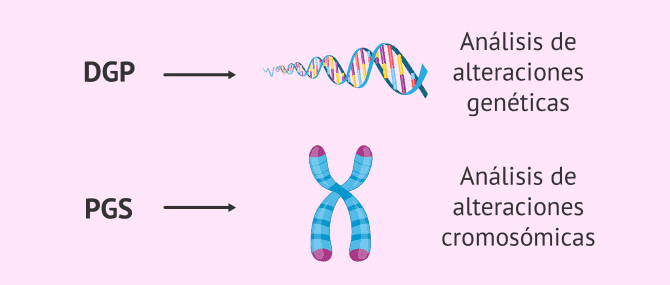
Aunque, en general, se utiliza el término diagnóstico genético preimplantacional o DGP para hacer referencia al uso de esta técnica, lo cierto es que se distinguen dos conceptos en función de la finalidad:
- Diagnóstico genético preimplantacional o DGP
- permite la detección precoz de enfermedades genéticas graves, las cuales pueden transmitirse a la descendencia si los padres son portadores o enfermos. Habitualmente, se trata de enfermedades hereditarias monogénicas como el Síndrome X-frágil, la enfermedad de Huntingon y la distrofia muscular.
- Cribado genético preimplantacional o PGS
- también llamado screening de aneuploidías. En este caso, se identifican alteraciones en el número o en la estructura de los cromosomas. La enfermedad cromosómica más conocida es el síndrome de Down.
En función de si se pretenden detectar alteraciones genéticas o cromosómicas en los embriones, las técnicas para el análisis del ADN embrionario serán diferentes.
¿Cuándo hacer un DGP?
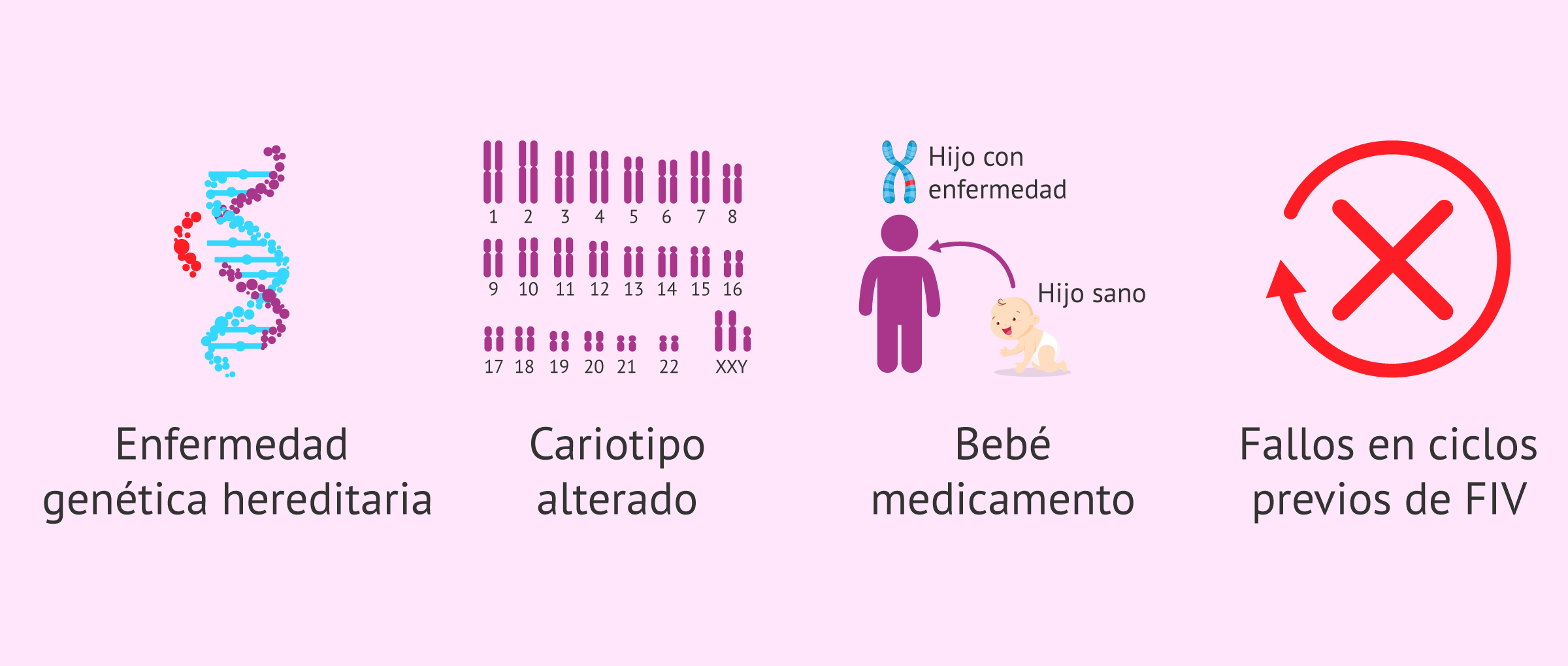
Los especialistas en genética y fertilidad aconsejarán llevar a cabo un DGP para tener un hijo en los siguientes casos:
- Cuando los progenitores, o al menos uno de ellos, son portadores de alguna enfermedad genética hereditaria.
- Cuando los progenitores, o al menos uno de ellos, tienen el cariotipo (estudio cromosómico) alterado. Por ejemplo, pueden ser portadores de translocaciones o inversiones cromosómicas.
- Cuando los progenitores ya tienen un hijo enfermo por alguna enfermedad que precisa un trasplante de células sanguíneas y deciden tener otro hijo sano y compatible. Es lo que se conoce como bebé medicamento.
- Después de varios fracasos repetidos en los ciclos de FIV.
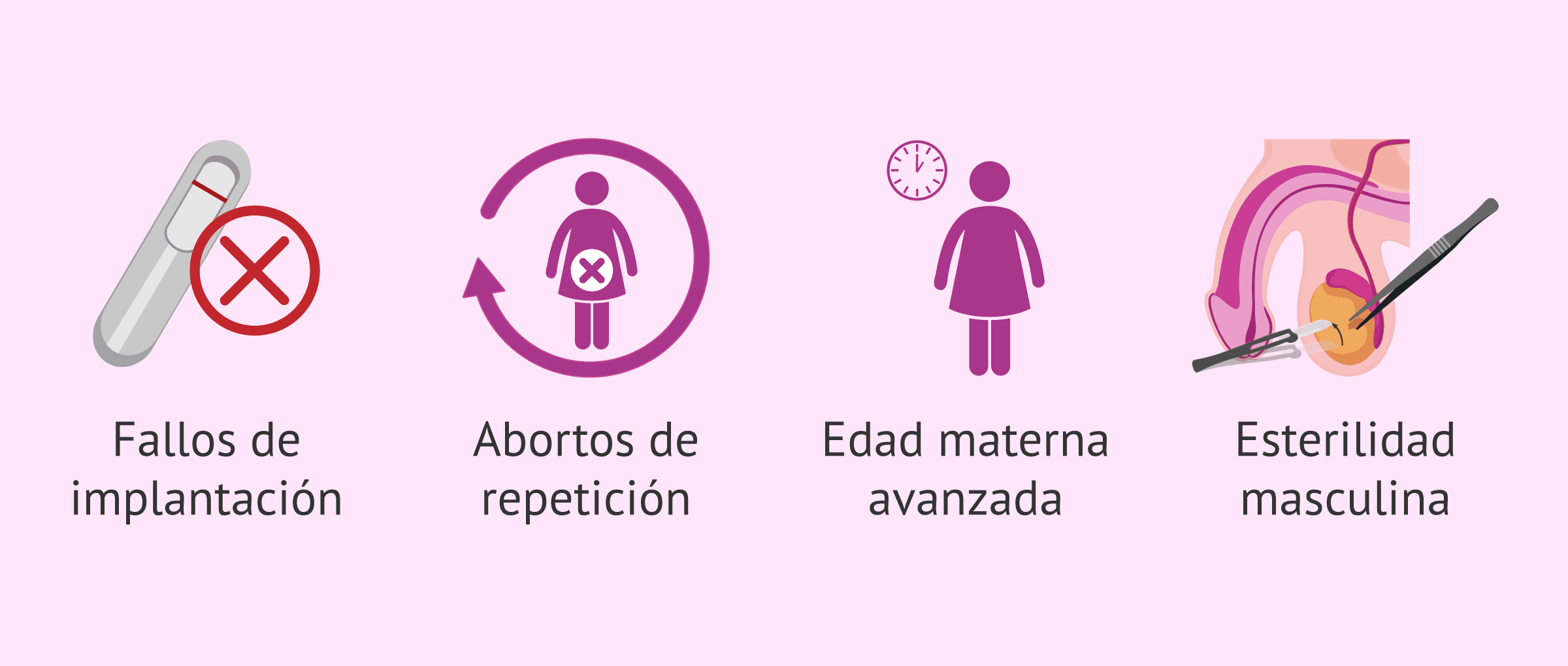
- Tras varios fallos de implantación embrionaria.
- Cuando existen abortos de repetición.
- Cuando la mujer tiene edad materna avanzada (se recomienda a mujeres de más de 38-40 años).
- Si hay antecedentes de un embarazo aneuploide (número incorrecto de cromosomas).
- En casos concretos de esterilidad masculina, cuando se requiere la obtención de espermatozoides del epidídimo o del testículo, por ejemplo.
Si quieres conocer en detalle las indicaciones y enfermedades genéticas que pueden detectarse mediante el DGP, puedes seguir leyendo aquí: Indicaciones del DGP.
Es posible calcular TU probabilidad de embarazo según el tratamiento, edad y otros factores?
Nos parece demasiado importante como para no compartirlo contigo.
Puedes personalizar tu informe de fertilidad en 2 minutos.
Procedimiento
Para poder hacer un DGP a los embriones, es necesario que la pareja o mujer se encuentre en un tratamiento de FIV. Por tanto, el primer paso es hacer una estimulación ovárica que permita obtener un número elevado de óvulos para fecundar.
Tras la punción ovárica para la obtención de los óvulos, se procede a fecundarlos mediante la técnica de ICSI (microinyección intracitoplasmática de espermatozoides) para la obtención de embriones.
El DGP puede hacerse tanto en embriones de 3 días en cultivo como en blastocistos de 5 días. En este último caso, es posible extraer un mayor número de células del trofoectodermo para hacer el estudio genético.
Los pasos para hacer el DGP en cada uno de los embriones son los siguientes:
- Biopsia embrionaria: se hace un agujero mediante un láser o sustancias químicas en la zona pelúcida del embrión para extraer una o dos células, si el embrión tiene 3 días, o varias células del trofoectodermo en el caso de los blastocistos.
- Tubing o entubado: las células extraídas se colocan en un tubo con mucha delicadeza. Posteriormente, se extraerá el material genético que contiene cada célula en su interior.
- Análisis del ADN extraído: existen varias técnicas como el FISH, el array de CGH, la PCR o la secuenciación.
- Valoración de resultados: se identifican los embriones genéticamente sanos y aquellos que presentan alteraciones en su material genético, los cuales serán descartados.
Por último, se valora la calidad de los embriones que sí son genéticamente viables para transferirlos al útero materno. Por otra parte, los embriones sobrantes se vitrificarán para futuros intentos.
Si quieres saber más sobre los pasos de este proceso, puedes acceder a este artículo: Procedimiento del DGP.
Tipos de PGT
Existen 3 tipos de análisis genético de los embriones en función del tipo de anomalía genética que se estudie. En el siguiente vídeo, Silvia Azaña, embrióloga en Reproducción Asistida ORG, nos cuenta las diferencias entre las distintas modalidades de PGT:
Tal y como cuenta Silvia en el vídeo:
El PGT-A evalúa si hay alteraciones cromosómicas numéricas o aneuploidías, es decir, si el número de cromosomas del embrión está alterado.
El PGT-M es el test indicado para evitar transmitir una enfermedad monogénica en concreto a la descendencia, cuando hay riesgo de que el bebé la padezca (porque existen antecedentes, un diagnóstico en los padres o ambos son portadores). El PGT-M (cuya M viene, por tanto, de enfermedades monogénicas, que afectan a un único gen).
En el caso del PGT-SR, la SR viene de reordenamientos estructurales en inglés, ya que analiza si hay alteraciones estructurales desequilibradas en los cromosomas del embrión.
Pros y contras
El DGP aplicado a la prevención de enfermedades hereditarias graves presenta un claro beneficio, pues evita que la pareja tenga que tomar la decisión de interrumpir o no el embarazo por llevar un bebé enfermo.
Por otra parte, el DGP para tratar la infertilidad y aumentar las tasas de éxito sí que da lugar a debate entre defensores y detractores de la técnica por las consideraciones éticas que implica.
A continuación, vamos a comentar las ventajas e desventajas del DGP, así como algunos aspectos éticos y legales.
Beneficios del DGP
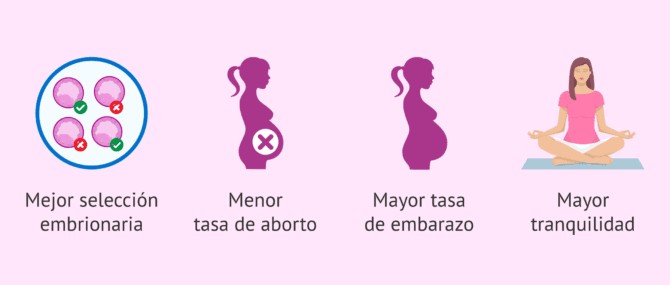
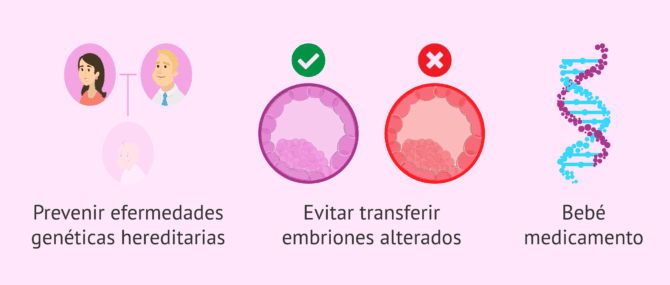
Las personas que deciden hacer un DGP durante la búsqueda del embarazo pueden lograr los siguientes beneficios:
- Mejor selección embrionaria
- evidentemente, el objetivo principal del DGP es detectar los embriones genéticamente sanos. Por tanto, ya directamente se pueden descartar aquellos con mutaciones o aneuploidias que, sin este análisis genético, podrían confundirse y transferirse a la madre, lo cual daría lugar a un fallo de implantación, aborto o nacimiento de niño enfermo.
- Menor riesgo de abortos
- algunas alteraciones cromosómicas permiten que el embrión implante, pero después de varias semanas de desarrollo acaban en un aborto espontáneo al no tener la dotación genética correcta.
- Mayor tasa de embarazo
- ya que se evitan los embriones que dan lugar a fallos de implantación repetidos.
- Menor número de tratamientos de FIV
- el DGP permite "acertar" en la selección del embrión con mayor capacidad de implantación y que puede dar lugar a un bebé sano. Por tanto, el número de transferencias fallidas se reduce, al igual que el tiempo para conseguir un embarazo.
- Mayor tranquilidad de los pacientes
- el DGP consigue eliminar la incertidumbre de si el embrión será bueno o no. Además, una vez conseguido el positivo, la mujer también se siente más relajada al saber que el embrión es viable y el riesgo de aborto mucho menor.
Tal y como hemos comentado previamente, aplicar la técnica de DGP reduce el número tratamientos de FIV. Además, esto también tiene la ventaja de que disminuye el coste económico invertido.
Es cierto que el DGP supone tener que pagar una cantidad de dinero adicional, pero también es posible que se produzca el embarazo antes que si no se aplicara el análisis genético.
Por tanto, en este caso, se estaría reduciéndose o evitándose, el coste que supondrían futuras transferencias embrionarias.
Inconvenientes del DGP
La aplicación del DGP también tiene, como el resto de técnicas de reproducción asistida, algunos inconvenientes:
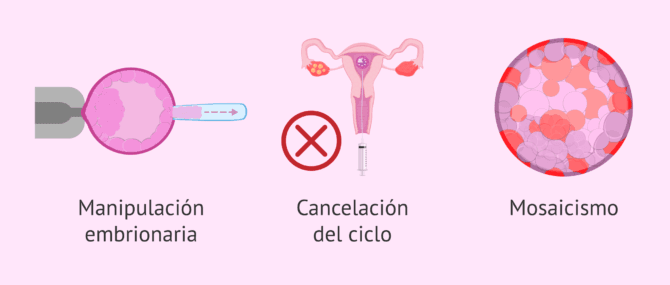
- Manipulación del embrión
- la biopsia embrionaria es un procedimiento invasivo que implica hacer un agujero en la zona pelúcida y, además, que éste pase más tiempo fuera del incubador. Algunos embriones no soportan este proceso y detienen su desarrollo.
- Cancelación del ciclo
- el DGP implica tener que descartar varios embriones por el resultado anómalo. Si la pareja no disponía de muchos embriones después de la fecundación, el riesgo de tener que cancelar la transferencia es mayor.
- Mosaicismo
- algunos embriones presentan mezcla de células normales y células alteradas. Por tanto, cuando solamente se biopsia una célula del embrión, es posible que se tome como sano un embrión mosaico no viable, o viceversa.
El resto de inconvenientes del DGP tienen que ver con aspectos éticos y morales, de los que hablaremos en el siguiente apartado.
Controversia ética del DGP
Algunas personas, por su creencia o religión, consideran que la vida empieza en el mismo momento de la fecundación. Por tanto, no están a favor de descartar embriones que podrían dar lugar a una vida, al igual que las personas que están en contra del aborto.
Por otra parte, tampoco consideran ético rechazar embriones que podrían dar lugar a niños con síndrome de Down, síndrome de Turner u otras enfermedades genéticas.
Estas son algunas de las cuestiones éticas y morales que entran en debate sobre el DGP y su aplicación:
- ¿Es ético seleccionar los embriones sanos y descartar los que porten una enfermedad?
- ¿Es ético seleccionar un embrión a fin de que cuando nazca pueda ayudar a curar alguna enfermedad de un familiar?
- ¿Es ético elegir el sexo del embrión o sus características físicas?
- ¿Las parejas sometidas a técnicas de FIV tienen derecho a conocer el genoma de sus embriones?
- ¿Es ético el DGP para enfermedades de aparición tardía?
- ¿Dónde está el límite en la selección genética de los embriones?
Precisamente por la controversia que genera, esta técnica reproductiva no está legalizada en muchos países y, si la ley la permite, generalmente se contemplan ciertas restricciones.
Aspectos legales del DGP
Gracias a la pionera Ley 14/2006 sobre Técnicas de Reproducción Humana Asistida, el diagnóstico genético preimplantacional es una técnica permitida en España. No obstante, para su aplicación es necesario que se cumplan algunos requisitos:
- En el caso de las enfermedades genéticas hereditarias, éstas deben ser consideradas como graves, de aparición temprana y sin ningún tratamiento curativo postnatal.
- En cuanto al resto de alteraciones cromosómicas, el DGP puede aplicarse para evitar la transferencia de embriones con viabilidad comprometida.
- Por último, el DGP puede utilizarse como método terapéutico para curar a un hijo enfermo (bebé medicamento), seleccionando los antígenos HLA de la futura descendencia. Esta práctica requiere una autorización expresa de la Comisión Nacional de Reproducción Humana Asistida (CNRHA).
La legalización del DGP en España ha permitido que nuestro país sea uno de los destinos principales para el llamado turismo reproductivo. Cabe destacar que el uso del DGP está muy restringido en países como Italia o Alemania.
Puedes seguir leyendo sobre este tema en el siguiente artículo: Turismo reproductivo para conseguir el embarazo.
¿Cuál es el precio del DGP?
El diagnóstico genético preimplantacional supone una complejidad añadida al proceso habitual de la fecundación in vitro, por lo que el coste económico es superior.
En general, el coste del DGP puede suponer unos 3.000-4.000€ adicionales al procedimiento de FIV-ICSI. Este precio de esta técnica complementaria dependerá de si se analizan únicamente los cromosomas básicos mediante FISH, los básicos con alguno adicional o todos los cromosomas.
Además, en el precio del DGP también influyen otros factores como la edad de la mujer, la técnica utilizada para el análisis, etc.
Si al comparar presupuestos lo haces solo mirando el precio final, es muy probable que no estés teniendo en cuenta aquello en el que las clínicas son menos claras.
Hemos creado esta guía de fertilidad para que entender los presupuestos sea muy sencillo y puedas compararlos sin sorpresas, ni abusos.
Normalmente, los centros de reproducción asistida suelen desglosar los presupuestos para que los pacientes puedan ver cuánto cuesta cada parte del tratamiento completo, además de la biopsia embrionaria y los estudios genéticos habituales.
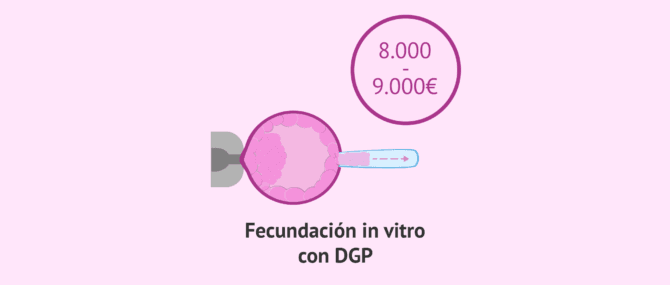
Cabe destacar que el precio final de un ciclo de FIV con DGP también depende de cada clínica de fertilidad y de cada caso en particular. No obstante, para hacerse una idea de su coste, el precio de una FIV con DGP se suele situar entre los 8.000€-9.000€.
Vídeo sobre el DGP
En el siguiente vídeo, la Dra. Ana Gaitero, directora médica de los centros HM Fertility Center, nos habla sobre el diagnóstico genético preimplantacional, sus indicaciones y procedimiento.
Tal y como dice en el vídeo:
Llamamos DGP al diagnóstico genético preimplantacional. Para hacerlo, necesitamos hacer embriones fuera del útero de la madre, cosa que hacemos en una fecundación in vitro o en una microinyección espermática. El objetivo es estudiar a los embriones mejor antes de ponerlos dentro de la madre.
Preguntas de los usuarios
¿Cuáles son los riesgos del PGT-A en mujeres de edad avanzada?
El diagnóstico genético preimplantacional (DGP o PGT) es una herramienta que nos permite estudiar las alteraciones cromosómicas y genéticas de un embrión antes de ser transferido al útero materno. Entre los principales riesgos del DGP se encuentran:
- Procedimiento invasivo.
- Existe la posibilidad de que todos los embriones estén alterados cromosómicamente.
- Saber si son embriones mosaicos.
- Asumir que la biopsia del embrión representa su totalidad.
- Aspectos éticos y emocionales.
¿Hay más posibilidad de que los embriones de buena calidad estén sanos tras un PGT?
La calidad embrionaria es un término complicado de definir. Por un lado, tendríamos la calidad “morfológica”, atendiendo a la disposición del trofoectodermo y la masa celular interna, y que nos da la clasificación por letras (A, B, C, D).
Sin embargo, que un embrión esté categorizado como A no implica que sea normal genéticamente hablando (lo que denominamos Euploide). Por lo tanto, podemos afirmar que la calidad morfológica no implica necesariamente una mayor probabilidad de resultar genéticamente normal tras realizar el PGT.
¿Es posible hacer DGP a los óvulos?
En la actualidad, no es posible hacer DGP a los óvulos. Esta técnica dañaría los óvulos y no sería posible fecundarlo para obtener embriones.
Leer más
¿Cuánto tardan los resultados del DGP?
El tiempo en el que se aportan los resultados del DGP suele ser de entre 2 y 4 semanas, aunque estos pueden variar según la técnica, el laboratorio de genética, etc. Asimismo, algunos laboratorios ofrecen la posibilidad de realizar un diagnóstico en 24h, aunque estos casos suelen estar estudiados, tanto por los costes como riesgos asociados.

Un aspecto importante es el caso en el que se precisa de un estudio genético previo para analizar enfermedades hereditarias. Estos casos suponen un estudio previo variable dependiendo de la patología y conocimientos sobre la enfermedad que puede llegar a los 2 meses. Después de ese periodo de tiempo se deberá realizar el tratamiento de reproducción asistida que concluirá con el diagnóstico genético. Es decir, que dicho proceso puede alargarse hasta los 4 meses.
¿Cuándo se recomienda hacer el PGT?
De modo general, realizar un test genético preimplantacional (PGT, antes llamado DGP) estaría aconsejado en situaciones como:
- Riesgo de transmitir una enfermedad genética al bebé, porque un progenitor padece una enfermedad genética de herencia dominante o ambos progenitores son portadores de mutaciones para una enfermedad genética recesiva.
- Cariotipo alterado en uno o ambos progenitores.
- Aborto de repetición.
- Fallos previos en ciclos de FIV.
- Edad de la mujer superior a 38-40 años, por el mayor riesgo de aneuploidías.
- Factor masculino severo, FISH de espermatozoides alterado o cuando se utilizan espermatozoides obtenidos del testículo o del epidídimo.

En cualquier caso, el equipo médico a cargo del tratamiento de reproducción asistida valorará cada caso particular para ver si realizar un PGT estaría indicado o no.
¿Cuál es el presente y el futuro del DGP?
En la actualidad, el DGP se ha convertido en una parte intrínseca de la medicina reproductiva y se suma a las opciones preventivas que se les ofrece a parejas con antecedentes personales o familiares de enfermedades hereditarias graves. También es útil como herramienta de mejora de las opciones reproductivas en grupos específicos de parejas con subfertilidad o riesgo incrementado para tener embriones con alteraciones cromosómicas.
El futuro del DGP busca integrar los nuevos conocimientos y desarrollos en metodologías de alto rendimiento genético, como las plataformas de ultrasecuenciación de nueva generación, junto con los avances en técnicas de reproducción asistida (TRA) para conseguir mejorar las opciones reproductivas de todas las parejas que acuden a las clínicas de reproducción asistida.
¿Hasta qué punto es importante la aplicación del DGP en mujeres que deciden ser madres en edad avanzada?
Desde punto de vista reproductivo, si fijamos como edad materna avanzada mujeres que buscan gestación a partir de 40-41 años, los datos clínicos son claros y revelan que los óvulos de estas mujeres presentan riesgo aumentado de alteraciones cromosómicas, especialmente trisomías como la del cromosoma 21 o Síndrome de Down.
Los datos clínicos de los principales grupos médicos que aplican el DGP muestran que su uso para este grupo de mujeres favorece la tasa de gestación y disminuye la tasa de aborto.
¿El DGP permite la selección del sexo del embrión?
María Hebles, responsable del laboratorio y embrióloga de Ginemed Sevilla nos responde. Tal y como nos dice María:
No. En España no es legal la selección de sexo, salvo aquellas enfermedades que vayan ligadas a los cromosomas sexuales, como, por ejemplo, la hemofilia. Si no, no podemos seleccionar embriones en función del sexo sin que no haya ninguna enfermedad indicada.
¿Por qué el PGT está indicado para mujeres de 40 años o más?
Con la edad de la mujer, la calidad de los óvulos va disminuyendo y es más probable que presenten alteraciones cromosómicas conocidas como aneuploidías.
Por ello, realizar un PGT (Test Genético Preimplantacional) a los embriones evitaría transferir al útero un embrión que presente alteraciones cromosómicas que podrían llevar a un aborto espontáneo o al nacimiento de un bebé con una enfermedad cromosómica como el síndrome de Down.
¿Cuántos embriones hay que tener para hacer un PGT?
Lo cierto es que no es necesario que haya un número mínimo específico de embriones para que sea posible realizar un test genético preimplantacional (PGT).
No obstante, en algunos casos en los que el número de embriones a analizar sea pequeño, puede ser recomendable comenzar una nueva estimulación ovárica para realizar una acumulación de embriones antes de realizar el PGT, puesto que se trata de una técnica costosa económicamente.
¿El PGT tiene algún riesgo?
Cuando se realiza un PGT (antes llamado DGP), el embrión puede ser dañado al realizar la biopsia embrionaria, pero la posibilidad de que esto ocurra es pequeña y la gran mayoría de embriones sobreviven al procedimiento.
Por otro lado, al recibir los resultados del PGT, puede ocurrir que ninguno de los embriones analizados haya obtenido un resultado favorable. En este caso, habría que cancelar el ciclo sin hacer transferencia embrionaria.
¿La biopsia embrionaria puede provocar alguna anomalía en el embrión?
La biopsia embrionaria se realiza en un momento temprano del desarrollo embrionario, por lo que el embrión tiene capacidad de seguir adelante y suplir esa pequeña cantidad de células extraída. Es cierto que el embrión puede dañarse con el procedimiento y que no sobreviva, pero esto es poco frecuente.
¿Hay alguna alternativa al PGT para evitar alteraciones genéticas?
Como alternativa al PGT (Test Genético Preimplantacional) para evitar alteraciones genéticas en la descendencia, podría realizarse alguna prueba de diagnóstico genético prenatal como la amniocentesis o la biopsia de vellosidades coriónicas.
No obstante, es importante tener en cuenta que, al tratarse de pruebas prenatales, se realizan cuando el embarazo ya se ha obtenido. Si el resultado muestra que el bebé tiene una alteración genética y no se desea continuar con el embarazo, habría que realizar una interrupción voluntaria del embarazo (IVE).

Finalmente, otra posible alternativa sería sustituir los gametos del progenitor o progenitores que portan la alteración genética por óvulos y/o espermatozoides de donante.
Lectura recomendada
Como hemos dicho, el DGP es una técnica complementaria que se lleva a cabo en el transcurso de una fecundación in vitro. Si quieres saber en qué consiste este tratamiento, puedes entrar en el siguiente post: ¿Qué es la FIV?
Para conocer información más detallada sobre los resultados del DGP y la probabilidad de éxito, puedes seguir leyendo en el siguiente artículo: Probabilidad de embarazo con el DGP.
Comunidad y Apoyo
En Reproducción Asistida ORG trabajamos para que la información mensual y rigurosa sea accesible para todos. Si este artículo te ha ayudado, considera apoyarnos para que podamos seguir acompañando a más personas en su camino hacia la maternidad y paternidad.
Bibliografía
Bick, D.P. y Lau, E.C. (2006). Diagnóstico genético preimplantacional. Pediatr. Clin. N. Am., 53: 559 – 577.
Delhanty, J.D.A. and Handyside, A.H. (1995) The origin of genetic defects in the human and their detection in the preimplantation embryo. Hum. Reprod. Update, 1, 201–215 (Ver)
Dokras, A., Sargent, I.L., Ross, C. et al. (1990) Trophectoderm biopsy in human blastocysts. Hum. Reprod., 5, 821–825 (Ver)
Ermanno Greco, Katarzyna Litwicka, Maria Giulia Minas, Elisabetta Cursio , Pier Francesco Greco, Paolo Barillari. Preimplantation Genetic Testing: Where We Are Today. Int J Mol Sci
. 2020 Jun 19;21(12):4381. doi: 10.3390/ijms21124381 (Ver)
Gleicher, N., Kushnir, V.A. & Barad, D.H. (2014). Preimplantation genetic screening (PGS) still in search of a clinical application: a systematic review. Reproductive Biology and Endocrinology, 12:22 (Ver)
Ilana Löwy. ART with PGD: Risky heredity and stratified reproduction. Reprod Biomed Soc Online. 2020 Nov 5;11:48-55. doi: 10.1016/j.rbms.2020.09.007 (Ver)
Manuel Viotti. Preimplantation Genetic Testing for Chromosomal Abnormalities: Aneuploidy, Mosaicism, and Structural Rearrangements. Genes (Basel). 2020 May 29;11(6):602. doi: 10.3390/genes11060602 (Ver)
Martine De Rycke, Veerle Berckmoes. Preimplantation Genetic Testing for Monogenic Disorders. Genes (Basel). 2020 Jul 31;11(8):871. doi: 10.3390/genes11080871 (Ver)
Moreno, J.M. (2007). Biopsia embrionaria. Aspectos técnicos. ASEBIR, 12: 17-21 (Ver)
Rodrigo, L.; Rubio, C.; Mateu, E. y Buendía, P., 2014. Capítulo 14: El laboratorio de diagnóstico genético preimplantacional. Instituto Universitario IVI Valencia. Máster en Biotecnología de la Reproducción Humana Asistida. 9ª Edición (2014-2016). 1213-1277
Preguntas de los usuarios: '¿Cuáles son los riesgos del PGT-A en mujeres de edad avanzada?', '¿Hay más posibilidad de que los embriones de buena calidad estén sanos tras un PGT?', '¿Es posible hacer DGP a los óvulos?', '¿Cuánto tardan los resultados del DGP?', '¿Cuándo se recomienda hacer el PGT?', '¿Cuál es el presente y el futuro del DGP?', '¿Hasta qué punto es importante la aplicación del DGP en mujeres que deciden ser madres en edad avanzada?', '¿En qué consiste el DGP o PGT?', '¿Puedo hacer DGP a los embriones sin tener una indicación clara?', '¿Qué pasos se siguen para hacer el DGP?', '¿Debo pasar por el comité si voy a una clínica privada para hacer un DGP?', '¿El DGP permite la selección del sexo del embrión?', '¿Por qué el PGT está indicado para mujeres de 40 años o más?', '¿Hay que hacer otros estudios prenatales si ya se ha hecho DGP?', '¿Cuántos embriones hay que tener para hacer un PGT?', '¿El PGT tiene algún riesgo?', '¿La biopsia embrionaria puede provocar alguna anomalía en el embrión?' y '¿Hay alguna alternativa al PGT para evitar alteraciones genéticas?'.
Autores y colaboradores












Hola
A fecha de hoy el DGP no está soportado en la seguridad social, mi pregunta es si posible realizar la In vitro por la SS y luego solicitar DGP (transferencia de Los embriones para estudio) a una clínica privada aunque tengamos que cubrir esa parte nosotros. Si es así, ¿existe alguna des ventaja o riesgo?
Saludos y ánimos para todas
Hola, el pasado lunes me hice la punción y me dijeron que uno de los embriones es 3PN. Me ha dicho de esperar 5 días para ver si evoluciona a blastocito y después analizarlo, que es un tipo de embrión que se suele descartar, pero que puede ser un embrión normal. He estado buscando información al respecto y me sale que suelen ser anómalos y por eso se descartan. ¿Puede ser porque la mayoría ha sido descartados? No sé bien qué hacer, ya no por lo económico, es el desgaste emocional.
¿Alguien me puede ayudar?