Un reciente estudio ha revelado hallazgos significativos sobre cómo la toxoplasmosis afecta a la salud reproductiva masculina. La investigación ha sido liderada por los autores Lisbeth Rojas-Barón, Leandro Tana-Hernandez, Mireille H. Nguele Ampama, Raúl Sanchéz, Ulrich Gärtner, Florian M. E. Wagenlehner, Christian Preußer, Elke Pogge von Strandmann, Carlos Hermosilla, Anja Taubert, María E. Francia y Zahady D. Velasquez.
Además, esta investigación ha sido posible por la colaboración de varias instituciones: Institute of Parasitology (Justus Liebig University Giessen, Alemania), Laboratory of Apicomplexan Biology (Institut Pasteur de Montevideo, Uruguay), Center of excellence in Translational Medicine Scientific and Technological Bioresource Nucleus y Department of Preclinical Sciences (Universidad de la Frontera, Chile), Institute of Anatomy and Cell Biology y Clinic for Urology, Pediatric Urology and Andrology (Justus Liebig University Giessen), EV-Core Facility (Philipps University Marburg, Alemania) y el Department of Parasitology and Mycology (Universidad de la Republica, Uruguay).
A continuación tienes un índice con los 6 puntos que vamos a tratar en este artículo.
Toxoplasmosis y fertilidad masculina
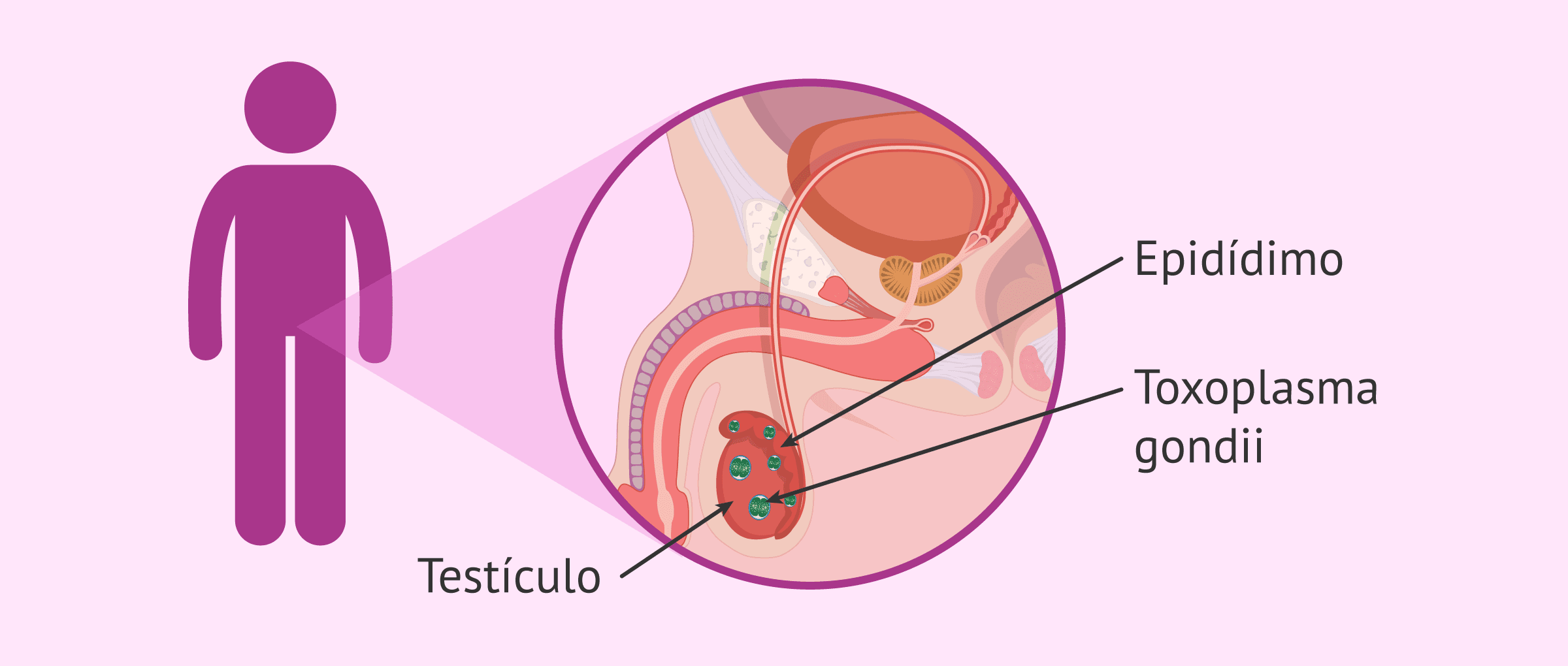
La infección aguda causada por el microorganismo Toxoplasma gondii puede tener consecuencias directas en la fertilidad del varón. Este parásito tiene la capacidad de infectar y proliferar directamente dentro de los testículos y el epidídimo, órganos fundamentales para la formación y maduración del semen.
Al colonizar estos órganos, el parásito altera la estructura habitual del tejido, provocando daño celular y permitiendo la infiltración de células del sistema inmunitario.
Esta capacidad del microorganismo para instalarse en la zona reproductiva es un hallazgo clave, ya que expone a las células reproductivas masculinas a un riesgo directo en etapas críticas de su desarrollo.
Daños directos en los espermatozoides
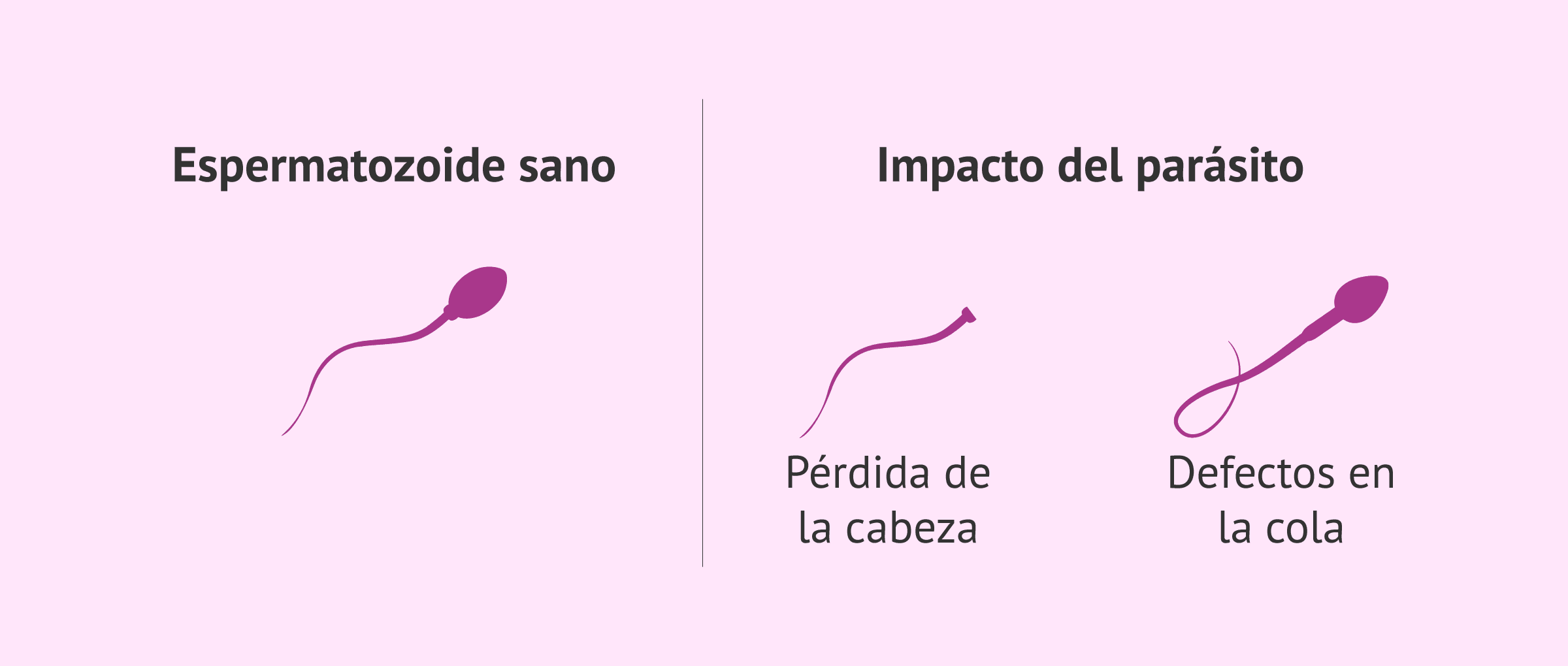
Uno de los descubrimientos más llamativos del estudio es que el parásito interactúa físicamente con los espermatozoides humanos, lo que provoca graves alteraciones. Entre los defectos estructurales más frecuentes destacan los siguientes:
- Una alta proporción de espermatozoides sin cabeza.
- Colas torcidas, dobladas en ángulo recto o enrolladas, lo que dificulta la movilidad natural del espermatozoide.
- Roturas (disrupciones) en la membrana plasmática que recubre la célula reproductiva.
Los investigadores han confirmado que este impacto sobre el espermatozoide no ocurre porque el parásito libere sustancias tóxicas al medio, sino que sería necesario un contacto o adherencia directa entre el microorganismo y la célula reproductora masculina.
Alteraciones en la función del esperma
Para lograr la fecundación, el espermatozoide necesita un gran aporte de energía proporcionado por sus mitocondrias, que funcionan como el motor de la célula. El estudio ha demostrado que la interacción con el parásito provoca una pérdida del potencial de membrana mitocondrial del espermatozoide. Esto lleva a la muerte celular, ya sea por apoptosis o necrosis.
A pesar de estos grandes daños estructurales y funcionales, la investigación indica que la infección no produce niveles anormales de oxidación (estrés oxidativo) en la muestra. Asimismo, se observó que el contacto con el parásito no incrementa la fragmentación del ADN del espermatozoide y tampoco altera, en un primer momento, la estructura de la cabeza encargada de perforar el óvulo, conocida como acrosoma.
Comunidad y Apoyo
En Reproducción Asistida ORG trabajamos para que la información mensual y rigurosa sea accesible para todos. Si este artículo te ha ayudado, considera apoyarnos para que podamos seguir acompañando a más personas en su camino hacia la maternidad y paternidad.
Bibliografía
Rojas-Barón L, Tana-Hernandez L, Nguele Ampama MH, Sanchéz R, Gärtner U, Wagenlehner FME, Preußer C, Pogge von Strandmann E, Hermosilla C, Taubert A, Francia ME, Velasquez ZD. Adverse impact of acute Toxoplasma gondii infection on human spermatozoa. FEBS J. 2025 Sep;292(17):4720-4736. doi: 10.1111/febs.70097. Epub 2025 May 3. PMID: 40318165; PMCID: PMC12414867. (Ver)