La gonadotropina coriónica humana (GCH), más conocida por sus siglas en inglés hCG o, incluso, coloquialmente por “la beta”, es una glucoproteína sintetizada en las células del trofoblasto embrionario. En concreto, la hormona hCG es producida por el sincitiotrofoblasto.
La hCG está formada por dos cadenas distintas, una alfa (α) y otra beta (ß). La cadena beta es exclusiva de la hormona hCG; mientras que la subunidad alfa es idéntica a la subunidad alfa de la hormona luteinizante (LH), foliculoestimulante (FSH) y hormona estimulante de la tiroides (TSH).
Las pruebas de embarazo se basan en detectar la subunidad beta de la hCG, puesto que es la parte específica. La presencia de esta hormona, al ser producida por el embrión, confirma la gestación. Además, por este motivo, al periodo de espera para la confirmación del embarazo se le llama comúnmente betaespera.
A continuación tienes un índice con los 11 puntos que vamos a tratar en este artículo.
- 1.
- 2.
- 3.
- 4.
- 4.1.
- 4.2.
- 4.3.
- 5.
- 6.
- 7.
- 7.1.
- 7.2.
- 7.3.
- 7.4.
- 7.5.
- 7.6.
- 8.
- 9.
- 10.
- 11.
¿Cuál es la función de la hormona hCG?
Después de la ovulación, los restos del folículo ovárico forman el cuerpo lúteo, que secreta progesterona. Si se produce un embarazo, la hormona hCG tiene como objetivo favorecer la funcionalidad de este cuerpo lúteo y es que, la hCG producida por el propio embrión, es un indicativo para que mantenga la secreción de progesterona hasta que la placenta se pueda ocupar de esta labor.
Por el contrario, en el caso de que no haya ocurrido un embarazo, la ausencia de hCG provoca que el cuerpo lúteo degenere, lo que finalmente desencadena la menstruación.
La hCG también podría intervenir en el desarrollo de la inmunotolerancia materna y, por tanto, impedir el rechazo inmunológico del embrión por parte de la madre durante el primer periodo de la gestación.
Además, como hemos comentado anteriormente, la subunidad alfa de esta hormona es idéntica a la de la LH y tienen cierta similitud biológica. Por ello, la hCG también se utiliza como fármaco para inducir la ovulación en los tratamientos de reproducción asistida.
Es posible calcular TU probabilidad de implantación según el tratamiento, edad y otros factores?
Porque sí, tener endometriosis, SOP, baja reserva ovárica, falta u obstrucción de las tompas, así como la calidad del semen condicionan tus probabilidades de embarazo.
Puedes personalizar tu informe de fertilidad en 2 minutos.
¿Por qué es útil detectar la hormona hCG?
La hCG es conocida también como la hormona del embarazo, pues su presencia es indicativa de gestación. De este modo, los test de embarazo se basan en evaluar la presencia de hormona hCG tanto en orina como en sangre.
Sin embargo, la detección de la beta hCG para confirmar el posible embarazo no se debe hacer hasta tener un retraso menstrual o hasta que hayan pasado, como mínimo, 15 días desde la relación sexual. Así, se da tiempo a que la hormona aumente a niveles detectables por la prueba.
Por otro lado, en los tratamientos de reproducción asistida se suele hacer la prueba de embarazo tras 10-15 días de betaespera desde la transferencia embrionaria o la inseminación artificial.
Además, niveles alterados de esta hormona pueden ser significativos de alteraciones genéticas en el feto, como síndrome de Down. Es por esto que los niveles de beta hCG libre se evalúan, junto con otros parámetros, en la prueba del triple screening que se realiza en el primer trimestre de embarazo.
Fármacos que contienen hCG
Como hemos mencionado, la hormona hCG también puede ser utilizada como fármaco en ciertas situaciones. En este caso, existen dos posibles formas de obtención de esta hormona para emplearla como tratamiento hormonal:
- hCG urinaria o u-hCG: obtenida a partir de la orina de mujeres gestantes y altamente purificada.
- hCG recombinante o r-hCG: obtenida por técnicas de ingeniería genética.
Sin embargo, con la introducción de la ingeniería genética y su evolución, el uso de la hCG de origen urinario quedó en un segundo plano.
Actualmente, el fármaco de hCG más común es el Ovitrelle, que contiene hCG recombinante.
Uso de hCG en reproducción asistida
La hormona hCG o gonadotropina coriónica humana es utilizada por mujeres que están realizando un tratamiento de reproducción asistida. Esta hormona se emplea para desencadenar la maduración final de los folículos y la ovulación.
El fármaco consiste en una inyección subcutánea que, de manera frecuente, se debe poner la propia paciente. La mujer recibirá una serie de indicaciones por parte del ginecólogo, para que la administración se realice de forma correcta.
Es importante mencionar que esta hormona no debe ser utilizada sin la supervisión de un especialista en reproducción asistida.
Efectos de la hCG
La hCG tiene similitud en estructura y actividad biológica a la hormona luteinizante o LH. Además, ambas hormonas comparten el mismo receptor en las células de la teca y de la granulosa del folículo ovárico.
Por este motivo, con la administración exógena de hCG se "simula" el pico de LH preovulatorio que ocurre durante un ciclo menstrual normal. De este modo, la hCG inicia una cascada de reacciones que produce los siguientes efectos en la mujer:
- Maduración final de los folículos y degradación de la pared folicular.
- Expulsión del óvulo, es decir, la ovulación.
- Formación del cuerpo lúteo.
Por otro lado, hay que tener en cuenta que la hCG induce la ovulación alrededor de 36-40 horas después de su administración. Por tanto, en los tratamientos de fecundación in vitro (FIV) la punción ovárica se debe realizar antes de que se cumpla este tiempo.
Así, se captan los ovocitos maduros antes de que sean liberados a la trompa de Falopio, ya que esto es lo que ocurriría en cualquier ciclo menstrual.
Indicaciones de la hCG
El uso de esta hormona está indicado en mujeres que se someten a técnicas de reproducción asistida, ya que se utiliza para planificar y controlar cuándo se produce la liberación de los óvulos por parte del ovario, como hemos mencionado previamente.
No obstante, la administración de esta hormona también puede ayudar a mujeres que presentan problemas para ovular, como oligoovulación o anovulación.
En cualquier caso, la administración de esta hormona debe realizarse bajo supervisión médica y siguiendo todas las pautas establecidas.
Ventajas y desventajas del empleo de hCG
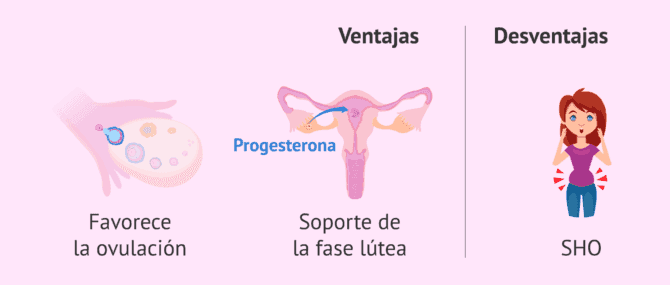
La principal ventaja de los fármacos con hCG es que esta hormona favorece la ovulación y, además, permite saber con exactitud el momento en el que esta se va a producir. Una vez transcurridas entre 36 y 40 horas desde la administración de la hCG, el óvulo será liberado.
Esto es sumamente importante en reproducción asistida, porque a partir de la inyección de hCG se programa el resto del tratamiento, ya sea la punción folicular o la inseminación.
Además, esta hormona sirve de soporte para la fase lútea. Esto quiere decir que la hCG mantiene la funcionalidad del cuerpo lúteo para la secreción de progesterona.
Sin embargo, el principal inconveniente del uso de hormona hCG en reproducción asistida es el riesgo de padecer el síndrome de hiperestimulación ovárica (SHO). La hCG tiene un efecto vasodilatador y puede provocar problemas graves de extravasación de líquidos si no se controla.
En este caso, podría resultar muy peligroso tener un embarazo con SHO agudo, ya que la hCG producida naturalmente por el embrión aumentaría los efectos perjudiciales.
Es por esto que, en aquellas situaciones en las que hay una elevada concentración de estrógenos antes de la punción ovárica, los embriones obtenidos se congelan y se transfieren en otro ciclo.
Esto es lo que recibe el nombre de transferencia en diferido y es una solución útil para los casos de SHO, ya que evita los riesgos de conseguir el embarazo en ese ciclo.
Efectos secundarios de la hCG
Como cualquier otro medicamento, la inyección de hCG también puede provocar algunas reacciones adversas. A continuación, se enumeran algunas de ellas:
- Dolor de cabeza.
- Dolor e hinchazón en el abdomen.
- Náuseas o, incluso, vómitos y diarrea.
- Síndrome de hiperestimulación ovárica (SHO).
- Dolor, hinchazón o irritación en el lugar de la inyección.
- Reacciones alérgicas, que se pueden manifestar con síntomas como erupción, lengua o boca hinchadas o dificultad para respirar.
- Problemas graves de coagulación sanguínea.
Si la paciente se encuentra en alguna de estas situaciones, lo mejor será consultar con un especialista lo antes posible para saber cómo proceder.
Vídeo sobre la hormona hCG
Silvia Azaña, embrióloga de Reproducción Asistida ORG, nos cuenta en este vídeo qué es la hormona hCG, sus funciones, por qué es útil detectarla y nos habla sobre su uso en reproducción asistida.
Tal y como dice Silvia en el vídeo:
La Gonadotropina Coriónica humana, muy conocida por sus siglas en inglés (hCG) y coloquialmente como la "hormona del embarazo" o, incluso, como la "beta", es una glucoproteína sintetizada en el trofoblasto embrionario.
Preguntas de los usuarios
¿Por qué tengo hormona hCG en sangre si no estoy embarazada?
La hormona hCG se produce casi con exclusividad en el tejido embrionario, y, es por ello, que se utiliza desde hace muchos años como el mejor marcador bioquímico de que la mujer está embarazada.
Ahora bien, ¿puede haber casos en los que la paciente tenga hCG elevada y no esté embarazada? En efecto, esto puede suceder, pero la mayor parte de estos casos son, en realidad, a causa de abortos o embarazos anormales como puede ser un embarazo bioquímico, un embarazo ectópico, etc.
Leer más
¿Para qué sirve la hormona del embarazo hCG?
La gonadotropina coriónica humana (hCG) es una hormona glicoproteica producida tanto por el embrión, como por el sincitiotrofoblasto, una parte de la placenta. La función de esta hormona es asegurar que el embrión recibe los factores nutricionales y hormonales, así como la protección necesaria para su correcto desarrollo.
Leer más
¿Cuáles son las causas de una hCG elevada en sangre?
La hCG es la hormona comúnmente conocida como la hormona del embarazo. Por tanto, elevados niveles de hCG en sangre sería indicativo de gestación. En función de cuál sea el valor exacto, se podrían determinar las semanas exactas.
¿Cuál es el mecanismo de acción de la hCG?
La finalidad de la hormona hCG es ejercer su función sobre el folículo, induciendo su maduración. Además, participa en la formación y el mantenimiento del cuerpo lúteo en el ovario.
Otro mecanismo de acción de la hCG es intervenir en la espermatogénesis, es decir, en la producción de espermatozoides en el caso de los hombres.
¿Se puede administrar hCG durante la lactancia?
No. La hormona hCG no está indicada en mujeres lactantes, ya que esta hormona es secretada en la leche.
¿Qué fármacos contienen hCG?
Con la aparición y el avance de las técnicas de ingeniería genética, la hCG urinaria quedó en un segundo plano y, en la actualidad, el fármaco con hCG más utilizado es el Ovitrelle, que contiene hCG recombinante.
Leer más
Lecturas recomendadas
Si deseas obtener información detallada acerca de los valores de beta hCG en el embarazo, no olvides visitar este artículo: ¿Cuáles son los valores normales de la hormona beta-hCG?
Si lo que te interesa es seguir leyendo acerca de las gonadotropinas, te recomendamos acceder a este enlace: Gonadotropinas: ¿Qué son y cuáles son sus funciones?
Comunidad y Apoyo
En Reproducción Asistida ORG trabajamos para que la información mensual y rigurosa sea accesible para todos. Si este artículo te ha ayudado, considera apoyarnos para que podamos seguir acompañando a más personas en su camino hacia la maternidad y paternidad.
Bibliografía
Abbara A, Clarke SA, Dhillo WS. Novel Concepts for Inducing Final Oocyte Maturation in In Vitro Fertilization Treatment. Endocr Rev. 2018 Oct 1;39(5):593-628. (Ver)
Choi J, Smitz J. Luteinizing hormone and human chorionic gonadotropin: distinguishing unique physiologic roles. Gynecol Endocrinol. 2014 Mar;30(3):174-81. (Ver)
Choi J, Smitz J. Luteinizing hormone and human chorionic gonadotropin: origins of difference. Mol Cell Endocrinol. 2014 Mar 5;383(1-2):203-13. (Ver)
Hay DL. Placental histology and the production of human choriogonadotrophin and its subunits in pregnancy. Br J Obstet Gynaecol. 1988 Dec;95(12):1268-75. (Ver)
Jameson JL, Hollenberg AN. Regulation of chorionic gonadotropin gene expression. Endocr Rev. 1993 Apr;14(2):203-21. (Ver)
Lawrenz B, Coughlan C, Fatemi HM. Individualized luteal phase support. Curr Opin Obstet Gynecol. 2019 Jun;31(3):177-182. (Ver)
Sirikunalai P, Wanapirak C, Sirichotiyakul S, Tongprasert F, Srisupundit K, Luewan S, Traisrisilp K, Tongsong T. Associations between maternal serum free beta human chorionic gonadotropin (β-hCG) levels and adverse pregnancy outcomes. J Obstet Gynaecol. 2016;36(2):178-82. (Ver)
Vaitukaitis JL, Braunstein GD, Ross GT. A radioimmunoassay which specifically measures human chorionic gonadotropin in the presence of human luteinizing hormone. Am J Obstet Gynecol. 1972 Jul 15;113(6):751-8. (Ver)
Wang Z, Gao Y, Zhang D, Li Y, Luo L, Xu Y. Predictive value of serum β-human chorionic gonadotropin for early pregnancy outcomes. Arch Gynecol Obstet. 2020 Jan;301(1):295-302. (Ver)
Ziolkowska K, Dydowicz P, Sobkowski M, Tobola-Wrobel K, Wysocka E, Pietryga M. The clinical usefulness of biochemical (free β-hCg, PaPP-a) and ultrasound (nuchal translucency) parameters in prenatal screening of trisomy 21 in the first trimester of pregnancy. Ginekol Pol. 2019;90(3):161-166. (Ver)
Preguntas de los usuarios: '¿Qué es la hCG?', '¿Cuál es la función de la hormona hCG?', '¿Por qué es útil detectar la hormona hCG?', '¿Para qué se usa la hCG en reproducción asistida?', '¿Cuáles son los efectos de la hCG exógena en la mujer?', '¿Cuáles son las indicaciones de la hCG?', '¿Qué ventajas y desventajas tiene el empleo de hCG en reproducción asistida?', '¿Qué efectos secundarios tiene la administración de hCG?', '¿Puede dar un test de embarazo positivo sin estar embarazada?', '¿Qué causa que la hCG aumente sus valores?', '¿Está indicada la hCG durante el embarazo y la lactancia?', '¿Por qué tengo hormona hCG en sangre si no estoy embarazada?', '¿Para qué sirve la hormona del embarazo hCG?', '¿Cuáles son las causas de una hCG elevada en sangre?', '¿Cuál es el mecanismo de acción de la hCG?', '¿Se puede administrar hCG durante la lactancia?' y '¿Qué fármacos contienen hCG?'.









Hoy he dado positivo con 3100. La transferencia fue el día 1. ¿No es un valor un poco alto?
Hola Helena82,
La verdad que sí es un valor bastante elevado de beta hCG si únicamente han pasado 15 días desde la transferencia embrionaria. Cuando vayas a la primera ecografía, tu médico te confirmará si se trata de un embarazo gemelar.
Espero haberte ayudado.
Un saludo.
Hola, estamos buscando el embarazo y hoy me he realizado una prueba de embarazo en casa y me ha salido positivo. Tengo dos días de retraso menstrual. ¿Me puedo fiar de ese resultado?
Buenos días Tham_lugo,
Los test de embarazo en orina son más fiables cuando se realizan una vez que ya se tiene un retraso en la menstruación. Por tanto, el resultado de la prueba es fiable y estás embarazada, ¡enhorabuena!
¡Que todo vaya bien!
Hola, tengo dolor de cabeza y muchas ganas de vomitar después de la inyección de hCG. ¿Alguna más ha sentido esto? ¿Es normal?
Buenos días 1984,
El dolor de cabeza y las náuseas están contemplados en los posibles efectos adversos que puede tener la inyección de hormona hCG. No obstante, si la molestia no remite o te preocupa, puedes consultar con el especialista que está llevando tu tratamiento, para asegurarte de que todo está bien.
¡Espero haberte ayudado!