La inyección intracitoplasmática de espermatozoides, abreviada como ICSI, es uno de los pasos de un tratamiento de fecundación in vitro (FIV). En concreto, la ICSI hace referencia al método de fecundación de los óvulos con los espermatozoides.
No obstante, muchas personas suelen utilizar el término ICSI o FIV-ICSI para referirse al proceso completo del tratamiento de fertilidad.
En el siguiente vídeo, la embrióloga Silvia Azaña te explica cómo es el tratamiento de ICSI paso a paso. No obstante, luego puedes profundizar con más detalle leyendo el artículo.
A continuación tienes un índice con los 7 puntos que vamos a tratar en este artículo.
- 1.
- 1.1.
- 1.2.
- 1.3.
- 1.4.
- 1.5.
- 1.6.
- 1.7.
- 1.8.
- 2.
- 3.
- 3.1.
- 3.2.
- 3.3.
- 3.4.
- 3.5.
- 3.6.
- 4.
- 5.
- 6.
- 7.
¿Cómo es el tratamiento de ICSI?
La ICSI tiene ciertos pasos que son completamente iguales al proceso de la FIV convencional. La diferencia entre los dos métodos radica en la forma en la que se produce la fecundación en el laboratorio una vez se han obtenido los óvulos y los espermatozoides.
A continuación, se describen cada una de las fases del tratamiento de la FIV-ICSI.
Estimulación ovárica controlada
La estimulación ovárica consiste en la administración de medicación hormonal para que varios folículos ováricos consigan madurar de forma simultánea. De esta manera, será posible obtener un número mayor de óvulos para fecundarlos en el laboratorio y aumentar la posibilidad de embarazo.
Además, gracias a la estimulación ovárica, se consigue controlar el ciclo menstrual de la mujer y evitar que tenga lugar la ovulación espontánea, lo cual haría fracasar el ciclo de FIV-ICSI.
Antes de empezar con la estimulación ovárica, el especialista puede indicar en algunos casos tomar la píldora anticonceptiva para poder controlar y sincronizar el ciclo menstrual de la mujer.
En función de la duración de la estimulación ovárica, existen dos protocolos básicos en las pacientes de FIV:
- Protocolo largo
- se inicia antes de la menstruación con los pinchazos de los fármacos agonistas de la GnRH, los cuales sirven para frenar la hipófisis y evitar la secreción de hormonas endógenas. Una vez llega la regla, se combinan los pinchazos anteriores con los de gonadotropinas para iniciar el desarrollo folicular múltiple.
- Protocolo corto
- el número de pinchazos se reduce, ya que la estimulación con gonadotropinas se inicia después de la llegada de la menstruación. Sobre el día 6-7 del ciclo, se empiezan a administrar los pinchazos con antagonistas de la GnRH para hacer el frenado hipofisiario.
En los últimos años, ha habido una tendencia a la simplificación de los protocolos de estimulación ovárica controlada.
La fase de administración de gonadotropinas (FSH) suele tener una duración aproximada de 6-10 días. Durante este tiempo, la paciente tendrá que acudir a control ecográfico unas 2 o 3 veces para comprobar el crecimiento folicular.
Puedes leer más sobre esta etapa del proceso en el siguiente enlace: ¿Qué es la estimulación ovárica?
Punción folicular
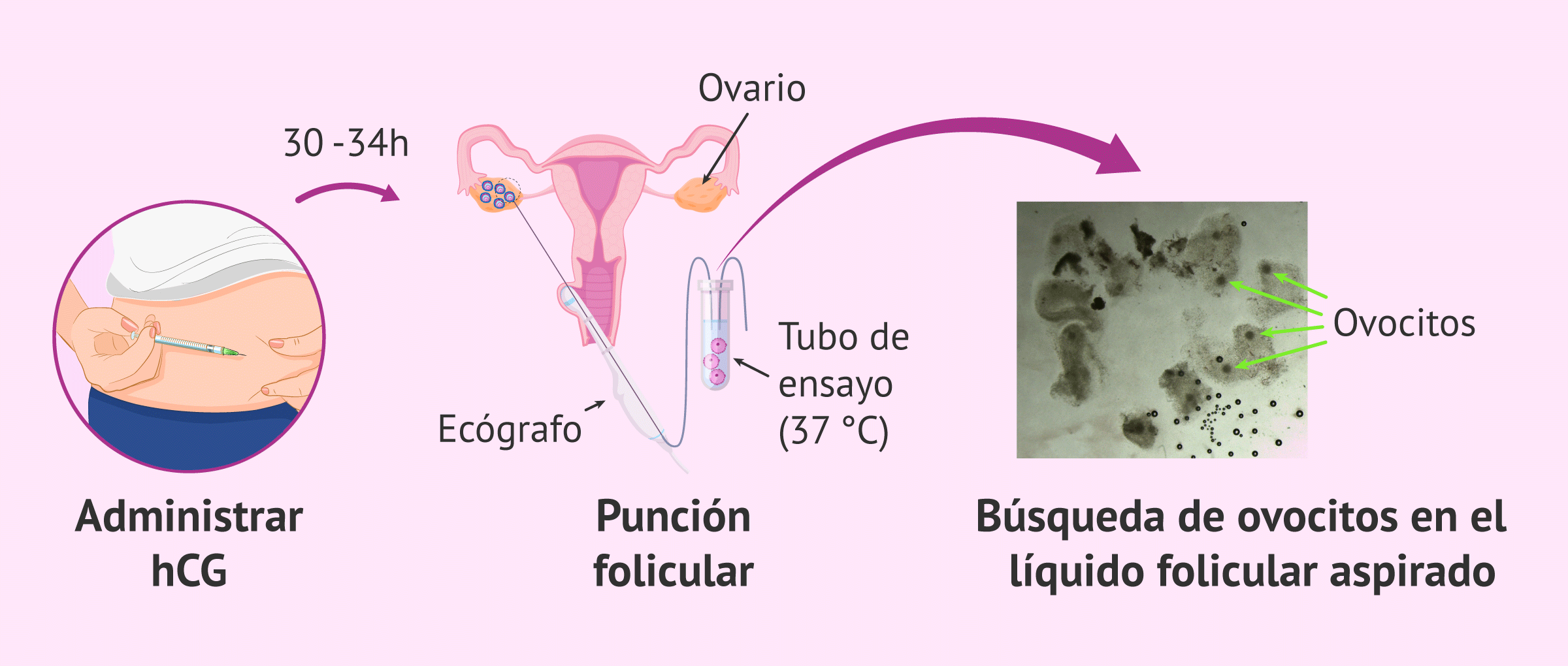
La punción folicular consiste en la aspiración del líquido contenido en los folículos ováricos para extraer los óvulos a través de una punción vaginal ecoguiada. Esto es una sencilla intervención de unos 30 minutos de duración que se realiza en el quirófano bajo anestesia, por lo que la paciente no siente dolor.
Unas 30-34 horas antes de la punción ovárica, la paciente debe administrarse una inyección de hormona hCG para desencadenar la ovulación e inducir la maduración final de los óvulos.
Una vez en el laboratorio, el líquido folicular aspirado debe examinarse detalladamente bajo la lupa para localizar los óvulos y trasladarlos a una placa con medio de cultivo.
Si te interesa conocer con más detalle esta fase del tratamiento, puedes seguir leyendo en el siguiente post: ¿Qué es la punción folicular de un proceso de FIV?
Decumulación de los óvulos
Esta etapa del proceso de la ICSI consiste en la eliminación de la capa de células de la granulosa que rodea al óvulo.
La decumulación de los óvulos, también conocida como denudación, es un paso necesario antes de hacer la microinyección intracitoplasmática de espermatozoides.
Para llevar a cabo el decumulado de los ovocitos, es necesario esperar unas horas después de la punción folicular porque el óvulo experimenta una maduración final durante este tiempo en reposo.
Existen dos técnicas para la decumulación ovocitaria:
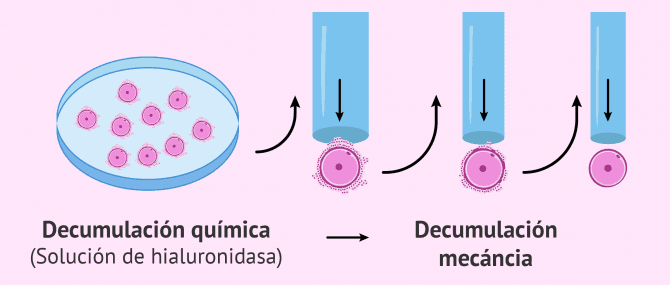
- Decumulación química
- se utiliza un medio con hialuronidasa, una enzima que degrada el ácido hialurónico que une las células de la granulosa entre sí. En la fecundación natural, la hialuronidasa es secretada por el espermatozoide para poder penetrar el óvulo.
- Decumulación mecánica
- el óvulo se va pasando por pipetas de diferente calibre, de mayor a menor diámetro, hasta despegar por completo todas las células que lo rodean.
Normalmente, los protocolos del laboratorio de FIV combinan ambos métodos para decumular los óvulos de manera más eficaz.
Después de la decumulación, hay que comprobar si los óvulos son maduros para poder hacer la ICSI. Para ello, es necesario visualizar un corpúsculo polar en el espacio perivitelino del óvulo.
Recogida y preparación del semen
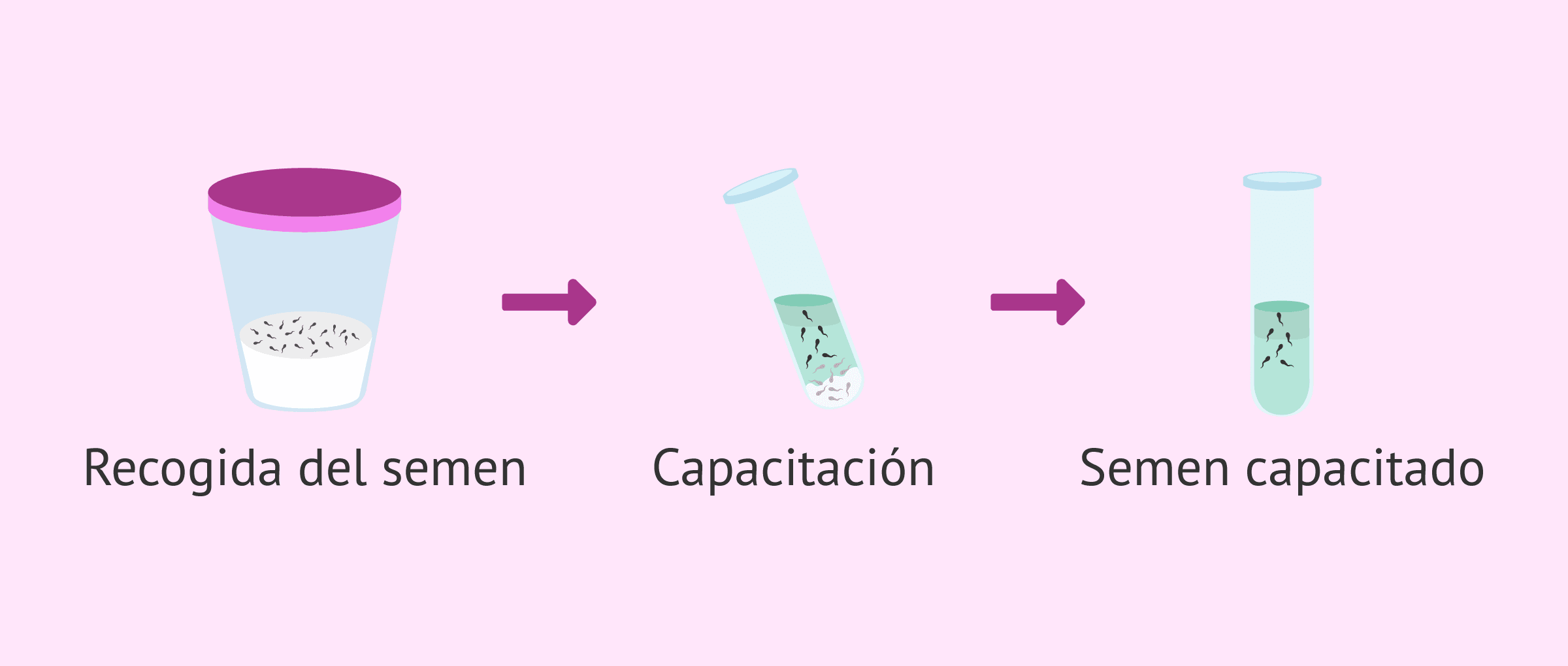
El mismo día de la punción folicular, el hombre debe dejar una muestra de semen en el laboratorio recogida por masturbación, a no ser que vaya a utilizarse semen congelado o de donante.
Para la preparación de la muestra seminal, es necesario hacer una capacitación espermática: se elimina el plasma seminal y se concentran los espermatozoides de mayor calidad en un medio de cultivo nuevo.
Existen varias técnicas para capacitar el semen. Puedes encontrar cómo se hacen detalladamente en el siguiente artículo: ¿En qué consiste la capacitación de los espermatozoides?
El objetivo es conseguir una muestra de espermatozoides móviles progresivos de un millón por mililitro aproximadamente, ya que si hubiera más espermatozoides sería difícil seleccionarlos bajo el microscopio.
Por otra parte, en los casos de factor masculino severo, es posible que se obtenga un menor número de espermatozoides y de peor calidad. De hecho, a veces es necesario obtener los espermatozoides con una biopsia testicular para hacer la ICSI.
No obstante, aunque sea más complicado, la ICSI también puede hacerse bajo estas condiciones, pues solamente son necesarios tantos espermatozoides vivos como óvulos se vayan a microinyectar.
Fecundación con ICSI
La manera de fecundar los óvulos es la que diferencia a la técnica de la ICSI de la FIV convencional.
Es posible calcular TU probabilidad de embarazo según el tratamiento, edad y otros factores?
Nos parece demasiado importante como para no compartirlo contigo.
Puedes personalizar tu informe de fertilidad en 2 minutos.
Como su propio nombre indica, la ICSI consiste en la inyección del espermatozoide directamente dentro del citoplasma del óvulo. Para ello, se siguen los siguientes pasos cuidadosamente:
- Preparación inicial
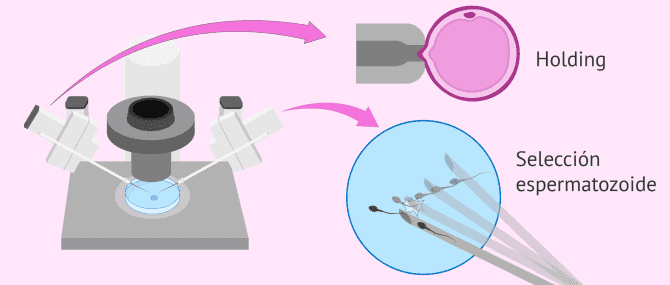
- se colocan las pipetas de sujeción (holding) y de microinyección (ICSI) en un microscopio invertido. A continuación, se prepara la placa de ICSI con gotas de medio de cultivo donde se colocarán los óvulos por una parte y los espermatozoides por otra.
- Selección del espermatozoide
- se observa la muestra de espermatozoides buscando el de mejor calidad y, una vez seleccionado, debe inmovilizarse con un movimiento rápido de la pipeta de ICSI para fracturar su cola. A continuación, se aspira el espermatozoide con esta misma pipeta.
- Orientación del óvulo
- para no dañar las estructuras internas del óvulo con la inyección, este se coloca orientado con su corpúsculo polar en la parte superior o inferior y es sujetado por la pipeta holding para que no se mueva.
- Inyección intracitoplasmática
- se presiona suavemente al óvulo con la pipeta de inyección para traspasar la zona pelúcida y la membrana interna. Una vez dentro del óvulo, se aspira un poco de citoplasma hasta ponerlo en contacto con el espermatozoide y, a continuación, se introduce suavemente en el interior del óvulo.
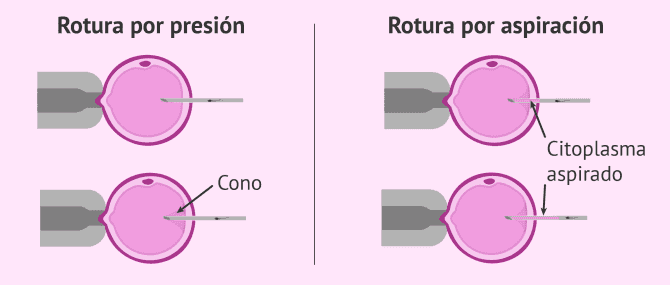
- Valoración final
- el tipo de rotura del óvulo aporta información sobre la calidad ovocitaria y puede condicionar su desarrollo posterior. El tipo de rotura puede ser por presión o por aspiración.
Por último, una vez microinyectados, se guardan los óvulos en placas de cultivo en el incubador, a la espera de valorar al día siguiente si ha habido fecundación.
En este vídeo, Silvia Azaña, embrióloga en Reproducción Asistida ORG, nos cuenta en detalle cómo se realiza una fecundación in vitro mediante ICSI:
Cultivo embrionario
Después de la fecundación y durante todo el desarrollo embrionario, es necesario valorar las características de los embriones con el objetivo de seleccionar aquellos de mejor calidad y con mayor posibilidad de implantar.
En función del estadio de desarrollo en el que se encuentre el embrión, se valorarán unos parámetros u otros:
- Cigotos
- se valoran unas 18 horas postfecundación para ver si han aparecido los dos corpúsculos polares y los dos pronúcleos, lo cual indicará que la fecundación ha tenido éxito.
- Embriones de 2-3 días
- el embrión ya se ha dividido y, por tanto, se valoran el número de células, su simetría, la fragmentación, la multinucleación, si hay vacuolas, etc.
- Blastocistos de 5-6 días
- en este estadio, el embrión ya está formado por multitud de células que forman la masa celular interna y el trofoectodermo. También se valora el grado de expansión de los blastocistos y si han empezado a salir de la zona pelúcida, lo cual se conoce como hatching.
Para más información sobre las condiciones y características del cultivo embrionario, puedes seguir leyendo en el siguiente post: Cultivo de embriones en el laboratorio de FIV.
Transferencia de los embriones
Teniendo en cuenta las circunstancias particulares de cada paciente y el número de embriones de buena calidad obtenido, la transferencia embrionaria puede realizarse en día 3 o en día 5 de desarrollo embrionario.
Para ello, se seleccionará el embrión o embriones de mejor calidad en base a los parámetros comentados. Puedes saber cómo se hace esta selección embrionaria en el siguiente enlace: Calidad embrionaria para la transferencia.
Antes de la transferencia embrionaria, la mujer suele administrarse progesterona para una óptima preparación endometrial.
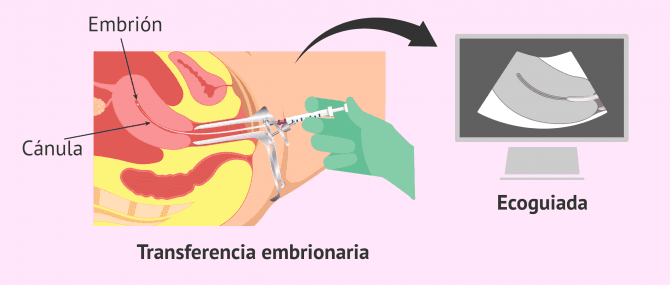
El procedimiento de transferencia embrionaria es muy sencillo y no requiere anestesia. En primer lugar, se coge el embrión seleccionado con un catéter fino y, seguidamente, se introduce por la vagina de la mujer hasta llegar al útero. Gracias a la ecografía que se hace simultáneamente, es posible ver cómo se deja al embrión en el útero con el objetivo de que se produzca la implantación.
Una vez depositado el embrión en el útero de la mujer, el personal del laboratorio comprobará la cánula bajo el microscopio para asegurarse de que el embrión no se ha quedado ahí.
En el siguiente artículo encontrarás todos los pasos detallados de la transferencia embrionaria después de un tratamiento de FIV: ¿Cómo se hace la transferencia de embriones?
Congelación de los embriones
En muchos ciclos de FIV quedarán embriones sobrantes después de la transferencia embrionaria, pues la legislación española solo permite transferir un máximo de 3 embriones.
Cada vez existe una tendencia mayor a transferir solamente un embrión en lugar de dos o tres. La principal razón es evitar la posibilidad de un embarazo múltiple y los riesgos que puede conllevar, tanto para la madre como para los fetos.
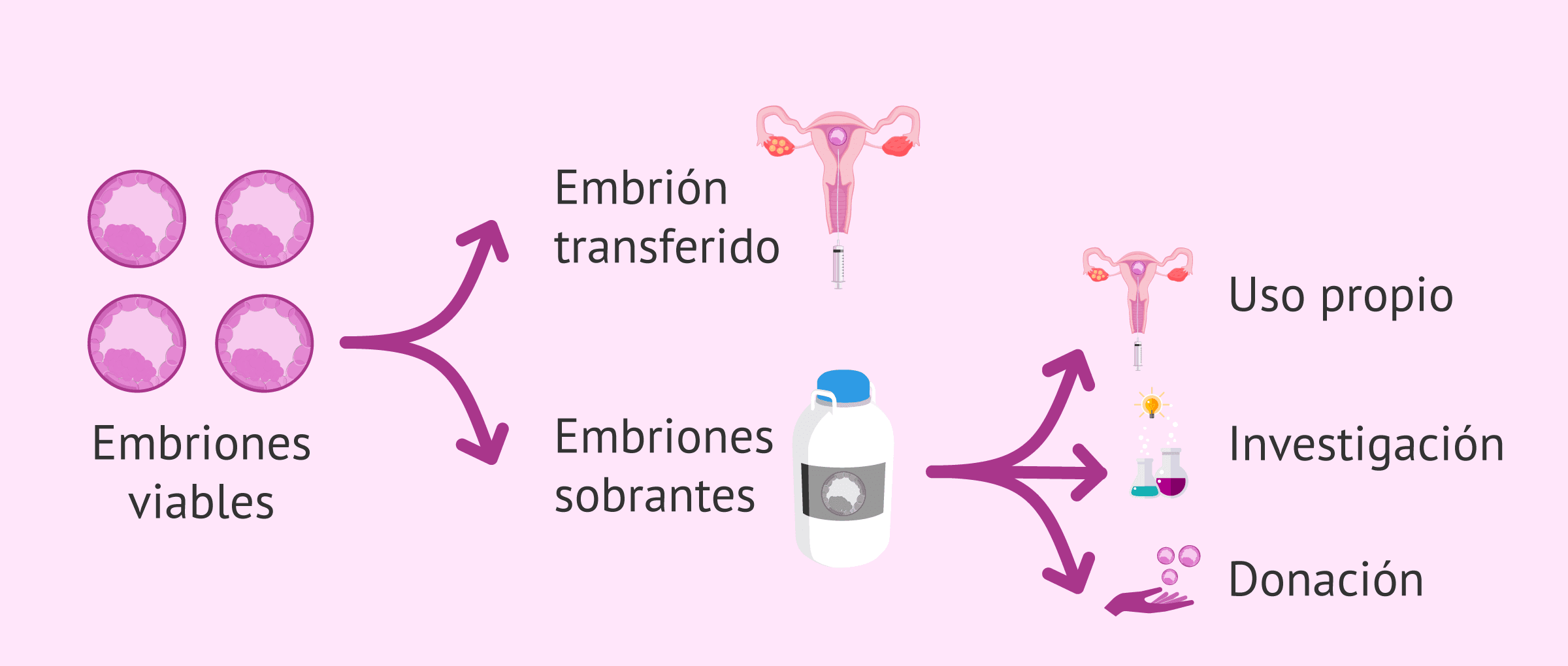
En consecuencia, los embriones que no son transferidos en el primer intento son vitrificados para usarlos en futuras ocasiones, bien porque la primera transferencia no ha tenido éxito, o bien para poder tener un segundo hijo en el futuro.
Para poder vitrificar los embriones, estos deben tener una calidad buena o media, de manera que se pueda garantizar la supervivencia de los embriones después de la desvitrificación.
Otra opción para los embriones sobrantes sería donarlos a otros pacientes o a la investigación.
Si quieres saber cómo son los protocolos de congelación en la actualidad, no te pierdas la lectura del siguiente post: ¿Qué es la vitrificación de embriones?
Test de embarazo después de la ICSI
La paciente deberá esperar alrededor de 9-12 días para hacer una prueba de embarazo y comprobar si la FIV-ICSI ha tenido éxito. Esta prueba se puede realizar en orina o en sangre, pero ambas se basan en detectar si hay presencia de beta hCG.
Por ello, comúnmente se conoce a este periodo de tiempo entre la transferencia embrionaria y la realización del test de embarazo como betaespera. La mayoría de los especialistas recomiendan seguir con la rutina diaria (sin realizar esfuerzos) durante la betaespera.
Preguntas de los usuarios
¿Qué es la ICSI?
El doctor José León Tovar, ginecólogo del centro Ginemed Huelva, nos responde en este vídeo:
La gran diferencia entre la FIV convencional y la ICSI es que en la ICSI cada óvulo es microinyectado con un espermatozoide. Entonces la fecundación, digamos que es como más controlada. No es un depósito de óvulos, un depósito de espermatozoides, sino que cada óvulo se le introduce un espermatozoide en su interior para evaluar la fecundación a las 24 horas.
¿Cuántos intentos de ICSI se recomienda hacer?
No existe ninguna contraindicación médica para un ciclo de ICSI repetido, por tanto, no se ha establecido un número máximo de intentos. Yo recomendaría realizar un total de tres intentos si no ha habido éxito durante los ciclos previos.
¿Es posible hacer una inyección intracitoplasmática de espermatozoides lentos?
Sí. En la ICSI es el embriólogo quien selecciona los espermatozoides y los microinyecta directamente en el óvulo. Siempre que sea posible, se elegirá un espermatozoide con buena movilidad y morfología, pero sería posible realizarlo con un espermatozoide que no se mueva de manera rápida. Lo que es aún más importante es la vitalidad espermática, es decir, que los espermatozoides estén vivos.
Leer más
¿Cuánto tiempo tarda en bajar la regla después de la punción?
Marta Barranquero, embrióloga en Reproducción Asistida ORG, nos habla en este vídeo acerca del tiempo que tarda en bajar la regla tras la punción folicular:
De manera natural, en un ciclo menstrual regular de 28 días de duración, la ovulación ocurre en torno al día 14 del ciclo y tu regla llega unas 2 semanas después.
Pues bien, en un ciclo de fecundación in vitro, se van a simular los tiempos de un ciclo natural. Por ello, la punción ovárica se hace unas horas antes de la ovulación, pero se considera como el día 14 del ciclo.
Así que tu regla llegará unas 2 semanas después de la punción ovárica. Sin embargo, debes tener en cuenta que la medicación que te administras durante la fase de estimulación ovárica puede causarte algún desajuste menstrual y por ello tu regla podría adelantarse o retrasarse algunos días. Esto es completamente normal.
¿Cuándo se hace el PGT después de la ICSI?
El test genético preimplantacional (PGT), antes conocido como DGP, es una prueba complementaria que consiste en el análisis genético de algunas células del embrión obtenidas mediante biopsia embrionaria. De este modo, es posible conocer si el embrión padece la alteración genética estudiada.
Lo más habitual actualmente es que la biopsia embrionaria se realice en día 5 de desarrollo embrionario, es decir, 5 días después de la ICSI.
Leer más
¿Cuándo es posible hacer un test de embarazo después de la ICSI?
Respetar los tiempo después de un tratamiento de fertilidad es fundamental para evitar llevarse sorpresas indeseadas. Por ello, da igual que se haga una FIV convencional o una ICSI, lo ideal es esperar al menos 10-12 días desde la transferencia embrionaria para hacerse una prueba de embarazo.

De esta manera, se reduce el riesgo de falso positivo o falso negativo. Además, cabe destacar que el análisis de la beta-hCG en sangre ofrece un resultado más preciso que el test de embarazo casero en orina.
Lecturas recomendadas
Si estás interesada en el tratamiento de ICSI y quieres obtener más información relacionada con esta técnica, te recomendamos visitar el siguiente artículo: ¿Qué es la FIV-ICSI?
Hemos comentado la tendencia actual de las clínicas de reproducción asistida a utilizar los protocolos simplificados de estimulación ovárica. Si quieres conocer con más detalle en qué consiste esto, puedes entrar en el siguiente post: ¿Qué es un protocolo corto con antagonistas de la GnRH?
La transferencia embrionaria puede hacerse en día 3 o en día 5, ya que ambas prácticas tienen una serie de ventajas e inconevnientes que deben valorarse en cada caso. Para saber más sobre este tema, te recomendamos seguir leyendo en el siguiente artículo: ¿Cuándo hacer la transferencia de embriones?
Comunidad y Apoyo
En Reproducción Asistida ORG trabajamos para que la información mensual y rigurosa sea accesible para todos. Si este artículo te ha ayudado, considera apoyarnos para que podamos seguir acompañando a más personas en su camino hacia la maternidad y paternidad.
Bibliografía
Campos G, Sciorio R, Esteves SC. Total fertilization failure after ICSI: insights into pathophysiology, diagnosis, and management through artificial oocyte activation. Hum Reprod Update. 2023 Jul 5;29(4):369-394. doi: 10.1093/humupd/dmad007. PMID: 36977357. (Ver)
Cutting E, Horta F, Dang V, van Rumste MM, Mol BWJ. Intracytoplasmic sperm injection versus conventional in vitro fertilisation in couples with males presenting with normal total sperm count and motility. Cochrane Database Syst Rev. 2023 Aug 15;8(8):CD001301. doi: 10.1002/14651858.CD001301.pub2. PMID: 37581383; PMCID: PMC10426261. (Ver)
Garrido N, Gül M, Jindal S, Vogiatzi P, Saleh R, Durairajanayagam D, Parmegiani L, Boitrelle F, Colpi GM, Agarwal A. How to select healthy sperm for intracytoplasmic sperm injection in samples with high sperm DNA fragmentation? Panminerva Med. 2023 Jun;65(2):148-158. doi: 10.23736/S0031-0808.23.04870-X. Epub 2023 May 16. PMID: 37194246. (Ver)
Jiang Y, Wang L, Wang S, Shen H, Wang B, Zheng J, Yang J, Ma B, Zhang X. The effect of embryo selection using time-lapse monitoring on IVF/ICSI outcomes: A systematic review and meta-analysis. J Obstet Gynaecol Res. 2023 Dec;49(12):2792-2803. doi: 10.1111/jog.15797. Epub 2023 Oct 1. PMID: 37778750. (Ver)
Sallam H, Boitrelle F, Palini S, Durairajanayagam D, Parmegiani L, Jindal S, Saleh R, Colpi G, Agarwal A. ICSI for non-male factor infertility: time to reappraise IVF? Panminerva Med. 2023 Jun;65(2):159-165. doi: 10.23736/S0031-0808.23.04869-3. Epub 2023 May 16. PMID: 37194245. (Ver)
Sciorio R, Fleming SD. Intracytoplasmic sperm injection vs. in-vitro fertilization in couples in whom the male partners had a semen analysis within normal reference ranges: An open debate. Andrology. 2024 Jan;12(1):20-29. doi: 10.1111/andr.13468. Epub 2023 Jun 7. PMID: 37259978. (Ver)
Yang L, Liang F, Zhu R, Wang Q, Yao L, Zhang X. Efficacy of intracytoplasmic sperm injection in women with non-male factor infertility: A systematic review and meta-analysis. Acta Obstet Gynecol Scand. 2024 Jan;103(1):30-41. doi: 10.1111/aogs.14698. Epub 2023 Nov 6. PMID: 37930100. (Ver)
Preguntas de los usuarios: '¿Qué es la ICSI?', '¿Cuántos intentos de ICSI se recomienda hacer?', '¿Es posible hacer una inyección intracitoplasmática de espermatozoides lentos?', '¿Cómo se realiza la estimulación ovárica controlada para una ICSI?', '¿Cuánto tiempo tarda en bajar la regla después de la punción?', '¿Cuándo se hace el PGT después de la ICSI?', '¿En qué consiste la punción ovárica del tratamiento de FIV-ICSI?', '¿Cuándo es posible hacer un test de embarazo después de la ICSI?', '¿Siempre se realiza la decumulación de los óvulos para una ICSI?', '¿Cómo se prepara la muestra de semen para una ICSI?', '¿Qué proceso se sigue para fecundar los óvulos mediante ICSI?', '¿Qué se valora durante el cultivo embrionario tras una ICSI?', '¿Cómo es la transferencia embrionaria en un tratamiento de FIV-ICSI?' y '¿Cuándo se realiza la congelación de embriones sobrantes en una ICSI?'.
Autores y colaboradores

Por otro lado, Montse estuvo de estancia en la Universidad Nacional de La Plata (Buenos Aires, Argentina). Más sobre Montserrat Villalobos Plumé







He llegado aquí buscando información para una FIV, ¿la ICSI es mejor? ¿Qué clínicas hacen ICSI en Sevilla?
Buenos días Tol91,
La técnica de ICSI es una técnica de fecundación in vitro (FIV), por la cual se microinyecta directamente un espermatozoide en el interior de un óvulo. Actualmente, la mayoría de clínicas de reproducción asistida utilizan la técnica ICSI para fecundar los óvulos cuando se hace un tratamiento de FIV, en lugar de realizar la técnica de FIV convencional para realizar este paso.
Por otro lado, si estás buscando una clínica de reproducción asistida en Sevilla para una FIV, te recomiendo acceder a nuestro Informe de Fertilidad. Contiene un listado de clínicas recomendadas en Sevilla por cumplir nuestros criterios de calidad, así como información de presupuestos y precios, muchísima información para cada paso de la FIV y una calculadora de tus probabilidades de éxito según el tratamiento, tu edad y otros factores.
¡Que vaya todo muy bien!
He leído sobre la ICSI y entiendo que se inyecta un espermatozoide directamente en el óvulo. Me cuesta imaginar cómo funciona en la práctica. ¿Es un proceso seguro para el óvulo y luego para el embrión?
Hola Canela,
Sí, la microinyección de espermatozoides o ICSI es una técnica segura y cada vez más utilizada en los centros de fertilidad como técnica de fecundación in vitro (FIV). Este procedimiento requiere precisión y manejo por parte del personal del laboratorio, pero la mayoría de los óvulos sobreviven y no resultan dañados tras la microinyección espermática. Por tanto, si los óvulos son fecundados correctamente, se podrán desarrollar los embriones.
Si deseas conocer más en profundidad esta técnica de FIV, puedes visitar el siguiente artículo: Microinyección espermática: ¿En qué consiste la ICSI y cuál es su precio?
Espero haberte ayudado.
Un saludo.